16.已知通过乙醇制取氢气有如下两条路线:
a.CH3CH2OH(g)+H2O(g)→4H2(g)+2CO(g)△H=+255.58kJ•mol-1
b.CH3CH2OH(g)+$\frac{1}{2}$O2(g)→3H2(g)+2CO(g)△H=+13.76kJ•mol-1
则下列说法不正确的是( )
a.CH3CH2OH(g)+H2O(g)→4H2(g)+2CO(g)△H=+255.58kJ•mol-1
b.CH3CH2OH(g)+$\frac{1}{2}$O2(g)→3H2(g)+2CO(g)△H=+13.76kJ•mol-1
则下列说法不正确的是( )
| A. | 降低温度,可提高b路线中乙醇的转化率 | |
| B. | 从能量消耗的角度来看,b路线制氢更加有利 | |
| C. | 乙醇可通过淀粉等生物质原料发酵制得,属于可再生资源 | |
| D. | 由a、b知:2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1 |
15.“活化分子”是衡量化学反应速率快慢的重要依据,下列对“活化分子”的说法中不正确的是( )
| A. | 活化分子之间的碰撞一定是有效碰撞 | |
| B. | 增大反应物的浓度,可使单位体积内活化分子增多,反应速率加快 | |
| C. | 对于有气体参加的反应增大压强,可使单位体积内活化分子增多,反应速率加快 | |
| D. | 催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加 |
14.下列判断错误的是( )
| A. | 离子半径:Na+>Mg2+>Al3+ | B. | 还原性:Cl->Br->I- | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
13.下列叙述正确的是( )
| A. | 同一周期中的ⅡA族和ⅢA族的原子序数之差一定为1 | |
| B. | 干冰晶体内存在共价键与分子间作用力 | |
| C. | 物质的熔、沸点高低顺序是Na2S>S>H2S>H2O | |
| D. | SiO2晶体和干冰的熔化过程中吸收热量都是为了克服分子间作用力 |
12.下列叙述中正确的是( )
| A. | ${\;}_{17}^{37}$Cl的中子数为37 | B. | H2O与D2O互称同素异形体 | ||
| C. | NH3的电子式为 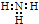 | D. | 1H与D互称同位素 |
11.下列说法正确的是( )
| A. | 纤维素从化学成分看,它是一种多糖.食物中的纤维素不仅能为人体提供能量,也能促进肠道蠕动、吸附排出有害物质 | |
| B. | 某物质的结构为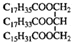 ,与其互为同分异构体,且完全水解后产物相同的油脂有3种 ,与其互为同分异构体,且完全水解后产物相同的油脂有3种 | |
| C. | 蛋白质的检验方法有许多种,而与双缩脲试剂作用而产生紫玫瑰色的颜色反应是最常见的方法之一 | |
| D. | 糖类、油脂、蛋白质是人类最主要的能量来源,它们都是天然高分子化合物 |
10.下列说法正确的是( )
| A. | 按系统命名法,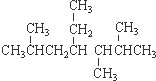 的名称为2,5,6-三甲基-4-乙基庚烷 的名称为2,5,6-三甲基-4-乙基庚烷 | |
| B. | 分子式为C5H12O且氧化产物能发生银镜反应的醇有6种 | |
| C. | 肌醇  与葡萄糖 与葡萄糖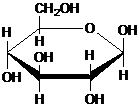 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 | |
| D. | 总物质的量一定时,乙炔和乙醛以任意比混合,完全燃烧消耗氧气量不变 |
9.下列说法正确的是( )
| A. | 试管、烧杯、表面皿、蒸发皿、圆底烧瓶都能用酒精灯直接加热 | |
| B. | 实验过程中若皮肤不慎沾上少量碱液,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗 | |
| C. | 通常用产生气泡的快慢,比较不同条件下Na2S2O3溶液与稀硫酸反应速率 | |
| D. | 当振荡分液漏斗中的混合溶液时,用右手压住分液漏斗的玻璃塞,左手握住旋塞,上下用力振荡 |
7.下列叙述中正确的是( )
0 173529 173537 173543 173547 173553 173555 173559 173565 173567 173573 173579 173583 173585 173589 173595 173597 173603 173607 173609 173613 173615 173619 173621 173623 173624 173625 173627 173628 173629 173631 173633 173637 173639 173643 173645 173649 173655 173657 173663 173667 173669 173673 173679 173685 173687 173693 173697 173699 173705 173709 173715 173723 203614
| A. | 酸碱中和滴定时眼睛要注视着滴定管内液面的变化,以防止滴定过量 | |
| B. | 在海轮外壳上绑上锌块,可减缓外壳腐蚀,这是应用外加电流的阴极保护法来防腐 | |
| C. | 在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,则水分解的热化学方程式为:2H2O (l)═2H2(g)+O(g△H=571.6kJ/mol | |
| D. | 增大反应物浓度,使活化分子百分数增加,化学反应速率增大 |