3.下列物质在水溶液中的电离方程式不正确的是:( )
| A. | Ca(OH)2═Ca2++2OH - | B. | Al2(SO4)3═2Al3++3SO42- | ||
| C. | NH4Cl═NH3+H++Cl- | D. | HNO3═H++NO3- |
1.I.有X、Y、Z、R四种短周期元素,Y、Z、R同周期.相关信息如下:
(1)Z元素在周期表的位置是第三周期第ⅦA族,Y、Z、R简单离子的半径从大到小的顺序是S2->Cl->Na+(用离子符号表示);
(2)由X、Z两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子里X、Z两种原子最外层均达到8个电子的稳定结构.甲遇水蒸气可形成一种常见的漂白性物质.则甲的结构式为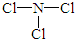 ;
;
(3)化合物乙(Y2R)溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质Y2R2,其溶液显黄色.写出乙溶液在空气中变质过程的化学方程式4Na2S+O2+2H2O═4NaOH+2Na2S2.
Ⅱ.元素X与氢可形成多种化合物,如丙、丁、戊.
(4)丙与醋酸类似,为一元弱酸,对热十分稳定但受撞击就爆炸.8.6g丙爆炸分解生成6.72L(标况下)X2和H2.写出其爆炸的化学方程式2HN3=3N2+H2;
(5)丁为离子化合物,遇水反应生成H2和气体戊,标况下戊的密度为0.76g•L-1,则物质丁的化学式为NH4H;
(6)戊在高温条件下能还原Fe2O3,产物中有两种单质,写出该反应的化学方程式2NH3+Fe2O3$\frac{\underline{\;高温\;}}{\;}$N2+2Fe+3H2O.
| 相关信息 | |
| X | 单质为双原子分子.若低温蒸发液态空气,因其沸点较低可先获得X的单质 |
| Y | 含Y元素的物质焰色反应为黄色 |
| Z | 同周期元素中原子半径最小 |
| R | R元素原子的最外层电子数是K层电子数的3倍 |
(2)由X、Z两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子里X、Z两种原子最外层均达到8个电子的稳定结构.甲遇水蒸气可形成一种常见的漂白性物质.则甲的结构式为
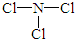 ;
;(3)化合物乙(Y2R)溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质Y2R2,其溶液显黄色.写出乙溶液在空气中变质过程的化学方程式4Na2S+O2+2H2O═4NaOH+2Na2S2.
Ⅱ.元素X与氢可形成多种化合物,如丙、丁、戊.
(4)丙与醋酸类似,为一元弱酸,对热十分稳定但受撞击就爆炸.8.6g丙爆炸分解生成6.72L(标况下)X2和H2.写出其爆炸的化学方程式2HN3=3N2+H2;
(5)丁为离子化合物,遇水反应生成H2和气体戊,标况下戊的密度为0.76g•L-1,则物质丁的化学式为NH4H;
(6)戊在高温条件下能还原Fe2O3,产物中有两种单质,写出该反应的化学方程式2NH3+Fe2O3$\frac{\underline{\;高温\;}}{\;}$N2+2Fe+3H2O.
20.某恒温密闭容器中,可逆反应A(s)?B+C(g)△H=+Q kJ•mol-1(Q>0)达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析不正确的是( )
| A. | 产物B的状态只能为固态或液态 | |
| B. | 平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1 | |
| C. | 若开始时向容器中加入1molB和1molC,达到平衡时放出热量小于Q kJ | |
| D. | 保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动 |
19.分枝酸可用于生化研究,其结构简式如图.下列关于分支酸的叙述正确的是( )
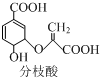

| A. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同 | |
| B. | 分子中含有2种官能团 | |
| C. | 可与乙醇、乙酸反应,且反应类型相同 | |
| D. | 1mol分枝酸最多可与3molNaOH发生中和反应 |
18.下列说法不正确的是( )
| A. | 过氧化钠、烧碱、纯碱分别属于碱性氧化物、碱、盐 | |
| B. | 乙醇和水可以任意比互溶,主要是因为乙醇和水分子间能形成氢键 | |
| C. | 硫酸钡、冰醋酸、酒精分别属于强电解质、弱电解质、非电解质 | |
| D. | 煤的气化、液化和干馏均属于化学变化 |
15.利用你学过的化学知识分析,下列反应的化学方程式错误的是( )
| A. | 2KNO3+S+3C═K2S+N2↑+3CO2↑ | |
| B. | 2KMnO4+3H2O2+3H2SO4═2K2SO4+2MnSO4+4O2↑+6H2O | |
| C. | 5KI+KIO3+6HCl═6KCl+3I2+3H2O | |
| D. | 4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑ |
14.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
0 173309 173317 173323 173327 173333 173335 173339 173345 173347 173353 173359 173363 173365 173369 173375 173377 173383 173387 173389 173393 173395 173399 173401 173403 173404 173405 173407 173408 173409 173411 173413 173417 173419 173423 173425 173429 173435 173437 173443 173447 173449 173453 173459 173465 173467 173473 173477 173479 173485 173489 173495 173503 203614
| A. | 标准状况下,22.4 LCCl4含有的分子数为NA个 | |
| B. | 500mL 1moL/L的盐酸溶液中含有的HCl分子数为0.5 NA个 | |
| C. | 将1L 2 mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA个 | |
| D. | 23gNa与O2反应生成Na2O和Na2O2的混合物,转移的电子数为 NA个 |
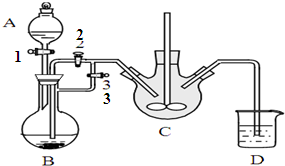 乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:
乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得: