7.下列关于FeCl2、FeCl3溶液和Fe(OH)3胶体的说法,错误的是( )
| A. | 三种分散系中分散质微粒都带电荷 | |
| B. | 加热蒸干并灼烧,得到的产物都是三氧化二铁 | |
| C. | FeCl2、FeCl3、溶液能稳定存在,而Fe(OH)3胶体不能稳定存在 | |
| D. | 一定条件下可完成转化:FeCl2溶液→FeCl3溶液→Fe(OH)3胶体 |
6.铝、铍(Be)及其化合物具有相似的化学性质,已知:BeCl2+Na2BeO2+2H2O═2NaCl+2Be(OH)2↓能完全进行,则下列推断正确的是( )
| A. | Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 | |
| B. | BeCl2水溶液的导电性强,故BeCl2是离子化合物 | |
| C. | Na2BeO2溶液的pH>7,将其蒸干并灼烧后得到的残留物为BeO | |
| D. | BeCl2溶液的pH>7,将其蒸干并灼烧后得到的残留物可能是BeCl2 |
5.含有N元素的化合物,下列关于判断错误的是( )
| A. | HNO3具有氧化性 | B. | NH3既具有氧化性又具有还原性 | ||
| C. | N2只具有还原性 | D. | NO2既具有氧化性又具有还原性 |
4.不考虑水的电离,下列水溶液中的四种离子可以大量共存,且物质的量浓度也相等的是( )
| A. | Na+、K+、MnO4-、NO3- | B. | ClO-、I-、NH4+、Ba2+ | ||
| C. | Na+、AlO2-、K+、HCO3- | D. | Al3+、K+、SO42-、NO3- |
3.下列物质按照单质、化合物、混合物顺序排列,其中物质类型排列顺序正确的是( )
| A. | 氯水、氯化钾、胆矾 | |
| B. | 液溴、水和冰混合、澄清石灰水 | |
| C. | 氮气、净化后的空气、氧化镁 | |
| D. | 白鳞、生锈的铁钉、高锰酸钾充分加热后的剩余固体 |
2.根据甲和乙两个对应的物理量,不能求出物质的量的是( )
| 选项 | 甲 | 乙 |
| A | 物质中的粒子数 | 阿伏加德罗常数 |
| B | 固体体积 | 固体密度 |
| C | 溶液中溶质的物质的量浓度 | 溶液体积 |
| D | 标准状况下气体摩尔体积 | 标准状况下气体体积 |
| A. | A | B. | B | C. | C | D. | D |
1.化学实验可以验证化学假说,获得化学事实.下列实验仪器常用于物质分离的是( )
①普通漏斗 ②量筒 ③蒸馏烧瓶 ④滴定管 ⑤分液漏斗 ⑥容量瓶.
①普通漏斗 ②量筒 ③蒸馏烧瓶 ④滴定管 ⑤分液漏斗 ⑥容量瓶.
| A. | ③⑤⑥ | B. | ②⑤⑥ | C. | ①③⑤ | D. | ②④⑥ |
20.下列装置能达到相应实验目的是( )
| A. |  验证碳酸的酸性强于硅酸 | B. |  分离苯和酒精 | ||
| C. |  制取少量O2 | D. |  收集少量NO2气体 |
19.二氧化锆是重要的耐高温材料、陶瓷绝缘材料.以锆英砂(主要成分为ZrSiO4,还含有少量的Fe203、Al2O3、SiO2等杂质)为原料制备二氧化锆(ZrO2)的工艺流程如图所示.
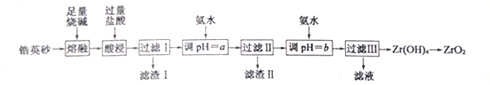
已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+.
②部分离子在实验条件下开始沉淀和完全沉淀时的pH如下表:
(1)经熔融后,锆英砂中Zr元素以Na2ZrO3(写化学式)形式存在.
(2)写出酸浸时生成Al3+、Fe3+的离子方程式Fe2O3+6H+=Fe3++3H2O,AlO2-+4H+=Al3++2H2O.
(3)滤渣Ⅰ的主要成分的名称为硅酸.
(4)向过滤Ⅱ所得滤液中加氨水调pH=b,则b的范围是5.2~6.2.
(5)向过滤Ⅲ所得的滤液中加入CaCO3粉末并加热,可得到CO2和另一种气体.该反应的离子方程式为2NH4++CaCO3=Ca2++2NH3↑+CO2↑+H2O.
(6)一种新型燃料电池,一极通入空气,另一极通入丁烷;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.在熔融电解质中,O2-向负(填“正”或“负”)极移动.负极电极反应为:C4H10-26e-+13O2-=4CO2+5H2O.

已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+.
②部分离子在实验条件下开始沉淀和完全沉淀时的pH如下表:
| 离子 | Fe3+ | Al3+ | ZrO2+ |
| 开始沉淀时pH | 1.9 | 3.3 | 6.2 |
| 完全沉淀时pH | 3.2 | 5.2 | 8.0 |
(2)写出酸浸时生成Al3+、Fe3+的离子方程式Fe2O3+6H+=Fe3++3H2O,AlO2-+4H+=Al3++2H2O.
(3)滤渣Ⅰ的主要成分的名称为硅酸.
(4)向过滤Ⅱ所得滤液中加氨水调pH=b,则b的范围是5.2~6.2.
(5)向过滤Ⅲ所得的滤液中加入CaCO3粉末并加热,可得到CO2和另一种气体.该反应的离子方程式为2NH4++CaCO3=Ca2++2NH3↑+CO2↑+H2O.
(6)一种新型燃料电池,一极通入空气,另一极通入丁烷;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.在熔融电解质中,O2-向负(填“正”或“负”)极移动.负极电极反应为:C4H10-26e-+13O2-=4CO2+5H2O.
18.下列图示实验合理的是( )

0 172080 172088 172094 172098 172104 172106 172110 172116 172118 172124 172130 172134 172136 172140 172146 172148 172154 172158 172160 172164 172166 172170 172172 172174 172175 172176 172178 172179 172180 172182 172184 172188 172190 172194 172196 172200 172206 172208 172214 172218 172220 172224 172230 172236 172238 172244 172248 172250 172256 172260 172266 172274 203614

| A. | 图4为用浓硝酸溶液与铜反应制备并收集少量NO2 | |
| B. | 图2为制备少量氧气 | |
| C. | 图3为配制一定物质的量浓度的硫酸溶液 | |
| D. | 图1为证明非金属性强弱:S>C>Si |