2.已知①I2+S02+2H20═H2SO4+2HI.②2FeCl2+Cl2═2FeCl3.③2FeCl3+2HI═2FeCl2+2HCl+I2,下列判断正确的是( )
| A. | 氧化性:FeCl3>Cl>I2 | B. | 氧化性:Cl2>FeCl3>I2 | ||
| C. | 还原性:SO2>HI>FeCl2 | D. | 还原性:SO2>FeCl2>HI |
19.下列说法中不正确的是( )
①水分子的电子式为
②离子半径由小到大的顺序是:Mg2+<Na+<Cl-<S2-
③氮分子的电子式为
④只含有离子键的化合物才是离子化合物.
①水分子的电子式为

②离子半径由小到大的顺序是:Mg2+<Na+<Cl-<S2-
③氮分子的电子式为

④只含有离子键的化合物才是离子化合物.
| A. | ①② | B. | ③④ | C. | ①④ | D. | ②③ |
18.下列微粒中,中心原子含有孤电子对的是( )
| A. | SiH4 | B. | CCl4 | C. | H2O | D. | NH4+ |
16.1.0L KNO3和Cu(NO3)2的混合液中c(NO3-)=4.0mol•L-1.用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况下),则原混合液中c(K+)为( )
| A. | 0.5 mol•L-1 | B. | 1.0 mol•L-1 | C. | 1.5 mol•L-1 | D. | 2.0 mol•L |
14.为了测定某镁铝合金的成分,取14.7g合金完全溶于500mL 3mol/L的硫酸中,再加入400mL 8mol/L的氢氧化钠溶液充分反应,最后只产生一种沉淀.则关于该合金的测定过程的描述正确的是( )
0 172064 172072 172078 172082 172088 172090 172094 172100 172102 172108 172114 172118 172120 172124 172130 172132 172138 172142 172144 172148 172150 172154 172156 172158 172159 172160 172162 172163 172164 172166 172168 172172 172174 172178 172180 172184 172190 172192 172198 172202 172204 172208 172214 172220 172222 172228 172232 172234 172240 172244 172250 172258 203614
| A. | 该合金中含有铝的质量至少为5.4 g | |
| B. | 合金中镁的质量分数为63.3%≤Mg%<100% | |
| C. | 在产生沉淀后的溶液中一定含有0.2 mol NaAlO2 | |
| D. | 在产生沉淀后的溶液中有1.6 mol Na2SO4 |
 羟胺(NH2OH)是一种不稳定的白色大片状或针状结晶.极易吸潮,极易溶于水,在热水中易分解.回答下列问题:
羟胺(NH2OH)是一种不稳定的白色大片状或针状结晶.极易吸潮,极易溶于水,在热水中易分解.回答下列问题: .
.

 ,G的结构简式为
,G的结构简式为 .
. +2CH3OH$?_{△}^{浓H_{2}SO_{4}}$
+2CH3OH$?_{△}^{浓H_{2}SO_{4}}$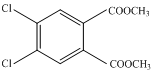 +2H2O.
+2H2O. .
.