12.下列物质中,既有离子键又有共价键的是( )
| A. | KOH | B. | CaCl2 | C. | H2O | D. | HF |
11.某一同学根据离子反应方程式2Fe3++Fe═3Fe2+来设计原电池.下列设计方案中可行的是( )
| A. | 电极材料为铁和锌,电解质溶液为FeCl3溶液 | |
| B. | 电极材料为铁和铜,电解质溶液为Fe(NO3)3溶液 | |
| C. | 电极材料为铁和石墨,电解质溶液为FeCl2溶液 | |
| D. | 电极材料为石墨,电解质溶液为FeCl3溶液 |
10.将金属钠分别投入下列物质的稀溶液中,有气体生成,且溶液质量减轻的是( )
| A. | 氢氧化钠 | B. | 硫酸 | C. | 氯化铜 | D. | 硫酸钠 |
9.1998年出现的全球温度大幅度升高,产生了显著的“厄尔尼诺”现象,干旱和暴雨灾难危害了许多地区.为了防止气候变暖的进一步恶化,联合国环境保护组织于1998年通过大会要求各国减少工业排放量的气体是( )
| A. | 二氧化硫 | B. | 二氧化碳 | C. | 氮的氧化物 | D. | 氟里昂 |
8.假设图中原电池产生的电压、电流强度均能满足电解、电镀要求,即为理想化.①~⑧为各装置中的电极编号.下列说法错误的是( )
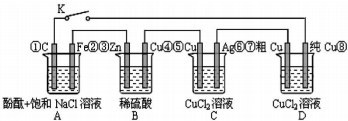

| A. | 当K闭合时,A装置发生吸氧腐蚀,在电路中做电源 | |
| B. | 当K断开时,B装置锌片溶解,有氢气产生 | |
| C. | 当K闭合后,整个电路中电子的流动方向为①→⑧;⑦→⑥;⑤→④;③→② | |
| D. | 当K闭合后,A、B装置中pH均变大 |
7.下列各组物质中,分子数相同的是( )
| A. | 2 L SO2和2 L CO2 | B. | 标准状况下1 mol氧气和 22.4 L水 | ||
| C. | 9 g水和标准状况下 11.2 LCO2 | D. | 0.1 mol氢气和 2.24 L氯化氢气体 |
6.a mol氢气分子和a mol氦气分子一定具有相同的( )
| A. | 原子数 | B. | 质量 | C. | 质子数 | D. | 体积 |
5.下列物质中,物质的量为0.5mol的是( )
| A. | 27g H2O | B. | 标准状况下,11.2L CO2 | ||
| C. | 6.02×1023个O2分子 | D. | 含0.5mol 氧原子的SO2 |
4.下列有关化学用语的表示正确的是( )
| A. | 钠原子的结构示意图为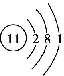 | B. | 过氧化氢的电子式为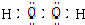 | ||
| C. | 聚乙烯的结构简式为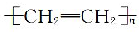 | D. | 淀粉和纤维素的实验式都为CH2O |
3.氯化钠是海水的主要成分,也是人类生活中不能缺少的一种物质.下列关于氯化钠的说法正确的是( )
0 171906 171914 171920 171924 171930 171932 171936 171942 171944 171950 171956 171960 171962 171966 171972 171974 171980 171984 171986 171990 171992 171996 171998 172000 172001 172002 172004 172005 172006 172008 172010 172014 172016 172020 172022 172026 172032 172034 172040 172044 172046 172050 172056 172062 172064 172070 172074 172076 172082 172086 172092 172100 203614
| A. | 氯化钠溶液能导电,所以氯化钠溶液是电解质 | |
| B. | 氯化钠溶液可杀菌,说明氯化钠溶液具有强氧化性 | |
| C. | 电解熔融氯化钠和电解氯化钠溶液的产物相同 | |
| D. | 加碘食盐是指添加了碘的化合物的氯化钠 |