19.潮湿的Cl2,新制的氯水,次氯酸能使有色布条褪色,其原因是这些物质中含有( )
| A. | HCl | B. | Ca(ClO)2 | C. | Cl2 | D. | HClO |
18.依据下表所列实验及现象得出的结论不正确的是( )
| 实验项目 | 实验现象 |
| FeCl3溶液中加入维生素C | 溶液褪色为浅绿色 |
| 饱和FeCl3溶液滴入沸水中 | 得到红褐色液体 |
| 将铜锈放入盐酸中 | 有无色气泡产生 |
| A. | 维生素C具有还原性 | B. | FeCl3水解生成Fe(OH)3胶体 | ||
| C. | 铜锈与盐酸反应有H2生成 | D. | 铜锈中含有碳酸根 |
17.下列有关物质的性质或应用正确的是( )
| A. | 实验室常用铝盐溶液与氢氧化钠溶液制备Al(OH)3沉淀 | |
| B. | 浓硫酸能干燥SO2、NO2等气体,说明浓硫酸具有吸水性 | |
| C. | SO2 具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色 | |
| D. | 30%的H2O2溶液中加入MnO2可制得O2,MnO2做氧化剂 |
14.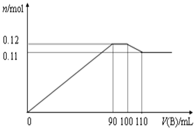 向100mLBaCl2、AlCl3、FeCl3 的混合溶液A中逐滴加入Na2SO4和NaOH的混合溶液B,产生沉淀的物质的量n和加入溶液B的体积关系如图所示:
向100mLBaCl2、AlCl3、FeCl3 的混合溶液A中逐滴加入Na2SO4和NaOH的混合溶液B,产生沉淀的物质的量n和加入溶液B的体积关系如图所示:
(1)当加入110mLB溶液时,溶液中的沉淀是BaSO4、Fe(OH)3(填化学式).
(2)溶液B中Na2SO4和NaOH的物质的量浓度之比是1:1.当B溶液加到90mL~100mL这一段时间中,所发生的离子反应方程式是Ba2++SO42-=BaSO4↓、Al(OH)3+OH-=AlO2-+2H2O
(3)将A、B溶液中各溶质的物质的量浓度(c)填入下表中.
 向100mLBaCl2、AlCl3、FeCl3 的混合溶液A中逐滴加入Na2SO4和NaOH的混合溶液B,产生沉淀的物质的量n和加入溶液B的体积关系如图所示:
向100mLBaCl2、AlCl3、FeCl3 的混合溶液A中逐滴加入Na2SO4和NaOH的混合溶液B,产生沉淀的物质的量n和加入溶液B的体积关系如图所示:(1)当加入110mLB溶液时,溶液中的沉淀是BaSO4、Fe(OH)3(填化学式).
(2)溶液B中Na2SO4和NaOH的物质的量浓度之比是1:1.当B溶液加到90mL~100mL这一段时间中,所发生的离子反应方程式是Ba2++SO42-=BaSO4↓、Al(OH)3+OH-=AlO2-+2H2O
(3)将A、B溶液中各溶质的物质的量浓度(c)填入下表中.
| 溶质 | Na2SO4 | NaOH | BaCl2 | AlCl3 | FeCl3 |
| c/mol•L-1 |
13.根据表中信息,判断下列叙述中正确的是( )
| 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 | |
| ① | Cl2 | FeBr3 | Cl- | ||
| ② | KMnO4 | H2O2 | H2SO4 | Cl2 | Mn2+ |
| ③ | KClO3 | 浓盐酸 | O2 |
| A. | 表中①组反应可能有一种或两种元素被氧化 | |
| B. | 表中②组反应的离子方程式是2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O | |
| C. | 表中③组反应的还原产物是KC1,电子转移数目是6e- | |
| D. | 氧化性强弱比较:KClO3>Fe3+>Cl2>Br2 |
10.下列离子方程式书写正确的是( )
0 171194 171202 171208 171212 171218 171220 171224 171230 171232 171238 171244 171248 171250 171254 171260 171262 171268 171272 171274 171278 171280 171284 171286 171288 171289 171290 171292 171293 171294 171296 171298 171302 171304 171308 171310 171314 171320 171322 171328 171332 171334 171338 171344 171350 171352 171358 171362 171364 171370 171374 171380 171388 203614
| A. | 氯气通入氯化亚铁溶液中:Cl2+Fe2+=2Cl-+Fe3+ | |
| B. | 碳酸钠溶于醋酸溶液中:CO32-+2 H+=H2O+CO2↑ | |
| C. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO | |
| D. | 硫酸与氢氧化钡溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |