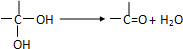
7.下列金属制品中最不容易被酸雨腐蚀的是( )
| A. | 镀锌水管 | B. | 铜制器皿 | C. | 铁制栏杆 | D. | 铝合金门窗 |
6.一定条件下,在体积为10L的固定容器中发生的反应:N2+3H2?2NH3,反应过程如图所示,下列说法正确的是( )

| A. | t1min时正、逆反应速率相等 | |
| B. | X曲线表示NH3的物质的量随时间变化的关系 | |
| C. | 0~8 min,H2的平均反应速率v(H2)=0.75 mol•L-1•min-1 | |
| D. | 10~12 min,N2的平均反应速率为v(N2)=0.25mol•L-1•min-1 |
5.用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如图,下列说法正确的是( )


| A. | 该物质属于烃类 | B. | 该物质易溶于水 | ||
| C. | 该物质能使酸性高锰酸钾溶液褪色 | D. | 该物质是一种高分子化合物 |
4.物质的量之比为1:3的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,下列说法正确的是( )
| A. | 在此反应中硝酸体现强氧化性,全部被还原 | |
| B. | 向反应后的溶液中再加入金属铁,不再发生化学反应 | |
| C. | 原混合物在反应后,被还原的硝酸与未被还原的硝酸之比为1:4 | |
| D. | 原混合物在反应后,被还原的硝酸与未被还原的硝酸之比为1:5 |
3.可逆反应N2O4?2NO2△H>0在密闭容器中反应,达到平衡状态,要使混合气体颜色加深,可采取的方法是( )
①选用合适的催化剂; ②缩小体积; ③升高温度; ④增大N2O4的浓度.
①选用合适的催化剂; ②缩小体积; ③升高温度; ④增大N2O4的浓度.
| A. | ③④ | B. | ①②③ | C. | ②③④ | D. | ①④ |
2.研究人员发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反
应可表示为:5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl 下列“水”电池在海水中放电时的有关说法正确的是( )
应可表示为:5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl 下列“水”电池在海水中放电时的有关说法正确的是( )
| A. | 正极反应式Ag+Cl--e-═AgCl | |
| B. | AgCl是还原产物 | |
| C. | Na+不断向“水”电池的负极移动 | |
| D. | 每生成1 mol Na2Mn5O10转移2 mol电子 |
20.下列叙述中,正确的是(NA代表阿伏加德罗常数)( )
| A. | 标准状况下,22.4L苯分子数为NA | |
| B. | 1mol•L-1FeCl3溶液中所含Cl-的数目为3NA | |
| C. | 25℃,1.01×105Pa,14g乙烯所含的碳原子数为NA | |
| D. | 1molNa2SO4溶于水,所得溶液中Na+的数目为NA |
19.对下列事实的解释错误的是( )
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硝酸在光照条件下颜色变黄,说明浓硝酸不稳定 | |
| C. | 常温下浓硫酸、浓硝酸可以用铝罐储存,说明浓硫酸、浓硝酸与铝不反应 | |
| D. | 反应CuSO4+H2S═CuS↓+H2SO4说明硫化铜既不溶于水,也不溶于稀硫酸 |
18.标况下,将4.8g铜和镁的合金溶于浓硝酸,同条件下测得反应中产生两种气体及体积分别为NO2(4.48L)、N2O4(0.336L),在反应后的溶液中,加入足量的NaOH溶液,则生成的沉淀总质量为( )
0 170899 170907 170913 170917 170923 170925 170929 170935 170937 170943 170949 170953 170955 170959 170965 170967 170973 170977 170979 170983 170985 170989 170991 170993 170994 170995 170997 170998 170999 171001 171003 171007 171009 171013 171015 171019 171025 171027 171033 171037 171039 171043 171049 171055 171057 171063 171067 171069 171075 171079 171085 171093 203614
| A. | 8.71g | B. | 8.86g | C. | 9.06g | D. | 7.04g |

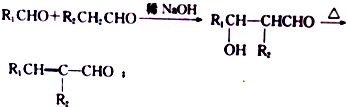
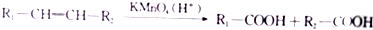
 .
. +(2n-1)H2O.
+(2n-1)H2O. (写出其中一种结构简式).
(写出其中一种结构简式).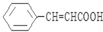 )的合成路线示意图.
)的合成路线示意图.