12.研究性学习小组进行了一系列化学实验后,发现高锰酸钾分解后的含锰元素的化合物都能和浓盐酸反应制得氯气,且锰化合物的还原产物都是MnCl2.他们将6.32g KMnO4粉末加热一段时间,也不知道高锰酸钾是否完全分解,收集到0.112L气体后便停止加热了,冷却后放入足量的浓盐酸再加热,又收集到气体体积是(上述气体体积都折合成标准状况)( )
| A. | 0.448L | B. | 2.016L | C. | 2.240L | D. | 无法确定 |
11.已知某H2SO4、FeSO4、Fe2(SO4)3混合液100mL,其中阳离子浓度相等,SO42-浓度为6mol/L,此溶液中还可溶解铁粉的质量为( )
| A. | 11.2g | B. | 16.8g | C. | 33.6g | D. | 5.6g |
10.磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性,制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的NaOH溶液,随后加入油酸钠溶液,即可生成黑色的、分散质粒子直径在36~55nm的磁流体.下列说法中正确的是( )
| A. | 所得的分散系属于悬浊液 | |
| B. | 所得的分散系中分散质为Fe2O3 | |
| C. | 该分散系能产生丁达尔效应且其中胶粒带正电荷 | |
| D. | 所得分散系为胶体,且胶粒直径即为氢氧化铁分子直径 |
9.有Xn-、Yn+、Z三种粒子,其电子层结构相同.下列分析正确的是( )
| A. | 粒子半径大小的关系是Xn-<Yn+ | B. | Z一定是稀有气体元素 | ||
| C. | 原子序数关系是:Z>Y>X | D. | 原子半径关系是:X>Y |
8.设NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 常温常压下,由x g NO2和y g N2O4组成的混合气体中原子总数为3NA,则x+y=46 | |
| B. | 1mol氯气参加氧化还原反应,一定得到2NA个电子 | |
| C. | 1L 0.1mol•L-1NaBr溶液中,HBr和Br-总和为0.1NA个 | |
| D. | 12.5mL 16mol•L-1浓硫酸与足量铜反应,生成SO2的分子数为NA |
7.下列反应的离子方程式正确的是( )
| A. | 铜片与AgNO3溶液反应:Cu+Ag+=Cu2++Ag | |
| B. | 铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 碳酸氢钠溶液和苛性钠溶液反应:HCO3-+OH-=CO32-+H2O | |
| D. | 氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
6.将4mol X气体和2mol Y气体在2L的密闭容器中混合并在一定条件下发生反应2X(g)+Y(g)?2Z(g),2s时测得Z的浓度为0.6mol/L.下列说法中不正确的是( )
| A. | 该反应达到平衡的标志是X的浓度不再发变化 | |
| B. | 升高温度能使该反应的速率加快 | |
| C. | 用物质Z表示的反应速率为1.2mol/(L•s) | |
| D. | 2s时Y的浓度为0.7mol/L |
5.下列措施不能增大相应反应的反应速率的是( )
| A. | Al在氧气中燃烧生成Al2O3,将Al片改成Al粉 | |
| B. | Fe与稀H2SO4反应生成氢气,改用浓H2SO4 | |
| C. | Cu与稀HNO3反应制NO,用酒精灯加热 | |
| D. | 在H2+I2?2HI的反应中,增大压强 |
4.某化学反应中生成物的总能量为80kJ,如果该反应是吸热反应,那么反应物的总能量可能是( )
0 170295 170303 170309 170313 170319 170321 170325 170331 170333 170339 170345 170349 170351 170355 170361 170363 170369 170373 170375 170379 170381 170385 170387 170389 170390 170391 170393 170394 170395 170397 170399 170403 170405 170409 170411 170415 170421 170423 170429 170433 170435 170439 170445 170451 170453 170459 170463 170465 170471 170475 170481 170489 203614
| A. | 120kJ | B. | 100kJ | C. | 90kJ | D. | 60kJ |
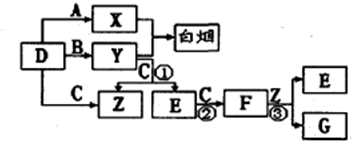 A、B、C、D是短周期元素形成的四种气体单质.E、F均为气体,且F为红棕色.有关的转化关系如图所示(反应条件均已略去).请回答下列问题:
A、B、C、D是短周期元素形成的四种气体单质.E、F均为气体,且F为红棕色.有关的转化关系如图所示(反应条件均已略去).请回答下列问题: