12.关于${\;}_{8}^{18}$O、${\;}_{8}^{16}$O、O2-、O四种微粒,以下说法正确的是( )
| A. | 它们是同种原子 | B. | 它们是几种不同单质 | ||
| C. | 氧元素的几种微粒的不同表示方法 | D. | 化学性质不同的几种氧原子 |
9.I.实验室制取氨气的常见方法如下:
(1)方法①的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(2)依据表中所列方法,从下图中选择合适的发生装置并将其序号填入表中装置栏中.

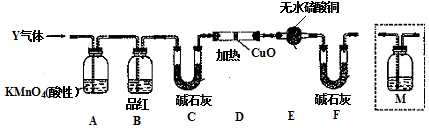
II.甲同学设计了下图所示实验装置(部分夹持仪器未画出),探究氨气的还原性并检验产物.

实验现象为:黑色CuO变为红色,白色无水CuSO4粉末变为蓝色,同时生成一种无色、无污染的气体.
(1)写出氨气与CuO反应的化学方程式3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.
(2)碱石灰的作用是吸收氨气中的水蒸气,防止干扰产物水的检验.
(3)该装置存在明显缺陷,应在上述装置最后连接一个尾气吸收装置,你认为可选用abd(填序号).

| 方法 | 装置 | |
| ① | 氯化铵与熟石灰固体混合加热 | |
| ② | 浓氨水加热 | |
| ③ | 浓氨水滴加到固体烧碱上 |
(2)依据表中所列方法,从下图中选择合适的发生装置并将其序号填入表中装置栏中.

II.甲同学设计了下图所示实验装置(部分夹持仪器未画出),探究氨气的还原性并检验产物.

实验现象为:黑色CuO变为红色,白色无水CuSO4粉末变为蓝色,同时生成一种无色、无污染的气体.
(1)写出氨气与CuO反应的化学方程式3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.
(2)碱石灰的作用是吸收氨气中的水蒸气,防止干扰产物水的检验.
(3)该装置存在明显缺陷,应在上述装置最后连接一个尾气吸收装置,你认为可选用abd(填序号).

7.下列关于苯的叙述正确的是( )
| A. | 苯分子为平面正六边形结构,6个碳原子之间的价键完全相同 | |
| B. | 从苯的凯库勒式( )看,苯分子中含有碳碳双键,应属于烯烃 )看,苯分子中含有碳碳双键,应属于烯烃 | |
| C. | 在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应 | |
| D. | 苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃 |
6.含有非极性键的离子化合物是( )
| A. | Na2O2 | B. | NaOH | C. | H2 | D. | HC1 |
5.下列说法中正确的是( )
| A. | HF、HCl、HBr、HI的热稳定性依次减弱,酸性依次减弱 | |
| B. | 熔融状态下能导电的化合物一定含离子键;金属与非金属元素形成的化合物一定是离子化合物 | |
| C. | NCl3分子中所有的原子均为8电子稳定结构 | |
| D. | NaHSO4晶体中阴、阳离子的个数是1:2且熔化时破坏的是离子键和共价键 |
4.今有一包铁粉和铜粉混合粉末,为确定其组成,现提供4mol/L的FeCl3溶液(其他用品略),某合作学习小组同学的实验结果如下(假定反应前后溶液体积不变)( )
| 组别 | ① | ② | ③ | ④ |
| V[FeCl3(aq)]/mL | 100 | 100 | 100 | 100 |
| 混合粉末质量/g | 6 | 13.2 | 24 | 36 |
| 反应后剩余固体质量/g | 0 | 1.28 | 12.8 | 24.8 |
| A. | 第①组溶液中c(Fe3+)=3.0 mol/L | |
| B. | 第②组剩余固体是铜铁混合物 | |
| C. | 第④组反应后的滤液中c(Fe2+)=6 mol/L | |
| D. | 原混合粉末中n(Fe):n(Cu)=3:2 |
3.下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中产物中一定不存在同分异构体的是( )
0 163872 163880 163886 163890 163896 163898 163902 163908 163910 163916 163922 163926 163928 163932 163938 163940 163946 163950 163952 163956 163958 163962 163964 163966 163967 163968 163970 163971 163972 163974 163976 163980 163982 163986 163988 163992 163998 164000 164006 164010 164012 164016 164022 164028 164030 164036 164040 164042 164048 164052 164058 164066 203614
| A. | 邻羟基苯甲酸与NaHCO3溶液反应 | |
| B. | 2-氯丁烷( )与NaOH的乙醇溶液共热 )与NaOH的乙醇溶液共热 | |
| C. | 甲苯在一定条件下发生硝化生成一硝基甲苯的反应 | |
| D. | 异戊二烯( )与等物质的量的Br2发生加成反应 )与等物质的量的Br2发生加成反应 |

 ,能证明凯库勒观点错误的实验现象是C中产生“喷泉”现象.
,能证明凯库勒观点错误的实验现象是C中产生“喷泉”现象.