17.下列说法不正确的是( )
| A. | 在铁制品上镀铜时,铁制品作电镀池的阳极,铜盐为电镀液 | |
| B. | 原电池工作时,电流的方向由正极→负载→负极→原电池中电解质溶液→正极 | |
| C. | 纯银在空气中久置变黑发生的是化学腐蚀 | |
| D. | 为避免船体遭受腐蚀,在船舶的外壳装上若干锌块,称为牺牲阳极的阴极保护法 |
16.枸椽酸乙胺嗪可用于驱除肠道虫病,其结构简式为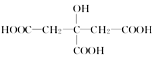 ,下列物质中不能与枸椽酸乙胺嗪反应的是( )
,下列物质中不能与枸椽酸乙胺嗪反应的是( )
 ,下列物质中不能与枸椽酸乙胺嗪反应的是( )
,下列物质中不能与枸椽酸乙胺嗪反应的是( )| A. | 乙酸 | B. | 乙醇 | C. | 溴的苯溶液 | D. | 氢氧化钠溶液 |
15.下列反应属于取代反应的是( )
| A. | 乙烯→聚乙烯 | B. | 乙酸→乙酸乙酯 | C. | 乙烯→乙醇 | D. | 乙醇→乙醛 |
14.下列燃料中,不属于化石燃料的是( )
| A. | 汽油 | B. | 煤 | C. | 氢气 | D. | 天然气 |
13.某同学为比较AgCl与Ag2S的溶解度大小,在室温下进行如下操作:
(1)操作1生成白色沉淀的离子方程式是Ag++Cl-?AgCl↓.
(2)进行操作2后,试管中白色沉淀转化为黑色沉淀,写出该反应的离子方程式2AgCl+S2-?Ag2S+2Cl-.
(3)通过上述现象可得到的结论是生成的AgCl沉淀中滴加Na2S溶液,可以转化为Ag2S沉淀.
(4)某同学认为,若将操作改为:
也能看到黑色沉淀生成,同样能得到(3)的结论,该同学说法是否正确,请说明理由不正确,若加5滴0.1mol/LNaCl溶液,反应后溶液中多余一定量的Ag+,再滴加Na2S溶液,也会产生Ag2S沉淀,不能说明是由AgCl沉淀转化而来.
(5)沉淀溶解原理在生产中也有重要用途.工业上利用双碱法除去SO2,其过程为用NaOH吸收SO2,并用石灰乳使NaOH再生,请结合化学用语解释用NaOH吸收SO2,SO2和NaOH溶液反应生成Na2SO3和H2O,加入石灰乳Ca(OH)2,石灰乳中存在化学平衡:Ca(OH)2?Ca2++2OH-,Ca2+与SO32-结合生成CaSO3,使化学平衡正向移动,产生NaOH,可以达到使NaOH再生的目的.
| 操作1 | 向盛有10滴 0.1mol•L-1 AgNO3溶液的试管中滴加0.1mol•L-1的NaCl溶液,至不再有白色沉淀生成. |
| 操作2 | 向上试管中滴加5滴0.1mol•L-1 Na2S溶液,静置 |
(2)进行操作2后,试管中白色沉淀转化为黑色沉淀,写出该反应的离子方程式2AgCl+S2-?Ag2S+2Cl-.
(3)通过上述现象可得到的结论是生成的AgCl沉淀中滴加Na2S溶液,可以转化为Ag2S沉淀.
(4)某同学认为,若将操作改为:
| 操作1 | 向盛有10滴 0.1mol•L-1 AgNO3溶液的试管中加5滴0.1mol•L-1NaCl溶液 |
| 操作2 | 向上试管中滴加5滴0.1mol•L-1 Na2S溶液,静置 |
(5)沉淀溶解原理在生产中也有重要用途.工业上利用双碱法除去SO2,其过程为用NaOH吸收SO2,并用石灰乳使NaOH再生,请结合化学用语解释用NaOH吸收SO2,SO2和NaOH溶液反应生成Na2SO3和H2O,加入石灰乳Ca(OH)2,石灰乳中存在化学平衡:Ca(OH)2?Ca2++2OH-,Ca2+与SO32-结合生成CaSO3,使化学平衡正向移动,产生NaOH,可以达到使NaOH再生的目的.
11.下列说法正确的是( )
| A. | 形成离子键的阴阳离子间只存在静电吸引力 | |
| B. | HF、HCl、HBr、HI的热稳定性和还原性均依次减弱 | |
| C. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 | |
| D. | 只要含有离子键的化合物就是离子化合物 |
10.下列试剂在空气中久置后,容易出现浑浊现象的是( )
| A. | 稀H2SO4 | B. | 稀硝酸 | C. | H2S溶液 | D. | 氨水 |
9.化学平衡状态是指( )
| A. | 反应不再发生 | |
| B. | 在一定条件下,反应混合物中各组成成分的浓度不随时间改变 | |
| C. | 反应容器内的总压强保持不变 | |
| D. | 反应物全部消耗 |
8.下列指定反应的离子方程式正确的是( )
0 163707 163715 163721 163725 163731 163733 163737 163743 163745 163751 163757 163761 163763 163767 163773 163775 163781 163785 163787 163791 163793 163797 163799 163801 163802 163803 163805 163806 163807 163809 163811 163815 163817 163821 163823 163827 163833 163835 163841 163845 163847 163851 163857 163863 163865 163871 163875 163877 163883 163887 163893 163901 203614
| A. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe═2 Fe3+ | |
| C. | 将铜插入稀硝酸中:Cu+4H++2NO3 -═Cu2++2NO2↑+H2O | |
| D. | 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+3H+═H2SiO3↓+3 Na+ |