题目内容
【题目】酒石酸托特罗定用于治疗泌尿系统疾病。工业合成该药物中间体(F)的路线如下:

己知:
回答下列问题:
(1)D分子中的含氧官能团名称为_________、_______________;B→C包含两步反应,反应类型分别为_______、______________。
(2)A的结构简式为______________________。
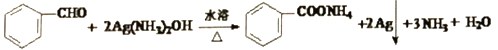
(3)写出苯甲醛与银氨溶液反应的化学方程式________________________________。
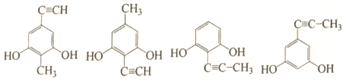
(4)B的一种同分异构体满足下列条件:①能使溴的CCl4溶液褪色;②能与FeCl3溶液发生显色反应;③分子中有4种不同化学环境的氢。写出该同分异构体的结构简式_______________。(任写一种)
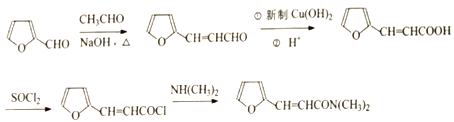
(5)已知呋喃丙胺(![]() CH=CHCON(CH3)2)是一种高效麻醉剂,写出以
CH=CHCON(CH3)2)是一种高效麻醉剂,写出以![]() 、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂自选)。合成路线流程图示例如下:_____________
、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂自选)。合成路线流程图示例如下:_____________
H2C=CH2![]() CHCH2Br
CHCH2Br![]() CH3CH2OH
CH3CH2OH
【答案】 羧基 醚键 加成 取代(酯化) ![]()
【解析】试题分析:(1)由D的结构简式可知,含有的含氧官能团为羧基、醚键;对比B、C结构可知,B与对甲基苯酚发生酯化反应,属于取代反应,甲基间位的C-H键断裂与碳碳双键发生加成反应形成六元环;
(2)由信息可知,对比苯甲醛与乙醛反应得到A为![]() ;
;
(3)苯甲醛与银氨溶液反应氧化反应得到苯甲酸铵、Ag、氨气与水,反应方程式为
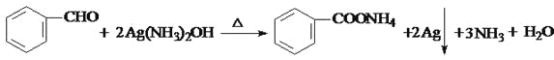 ;
;
(4)B的一种同分异构体满足下列条件:①能使溴的CCl4溶液褪色,说明含有不饱和键,可以是碳碳三键等,②能与FeCl3溶液发生显色反应,说明含有酚羟基,③分子中有4种不同化学环境的氢,符合条件的同分异构体有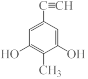
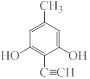
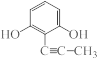
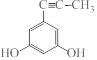 等;
等;
(5)![]() 与CH3CHO在氢氧化钠、加热条件下得到
与CH3CHO在氢氧化钠、加热条件下得到![]() ,再用新制氢氧化铜氧化、然后酸化得到
,再用新制氢氧化铜氧化、然后酸化得到![]() ,再与SOCl2发生取代反应得到
,再与SOCl2发生取代反应得到![]() ,最后与NH(CH3)2反应得到
,最后与NH(CH3)2反应得到![]() ,合成路线流程图为
,合成路线流程图为
 。
。

【题目】一定温度下,在三个恒容体积均为2.0L的容器中发生反应:PCl5(g) ![]() PCl3(g)+Cl2(g),下列说法正确的是( )
PCl3(g)+Cl2(g),下列说法正确的是( )
编号 | 温度(℃) | 起始/mol | 平衡/mol | 达到平衡 所需时间/s | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
Ⅱ | 320 | 0.80 | t2 | ||
Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
A. 平衡常数K:容器Ⅱ>容器Ⅲ
B. 反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ
C. 反应到达平衡时,容器I中的平均速率为v(PCl5)=0.1/t1 molL-1s-1
D. 容器Ⅲ中平衡后,等温条件下充入一定量He,平衡不发生移动