题目内容
【题目】X(s)+3Y(g)![]() Z(g) ΔH=-a kJ·molˉ1 ,一定条件下,将2mol X和2 mol Y通入2L的恒容密闭容器中,反应10s,测得生成0.5molZ。下列说法正确的是
Z(g) ΔH=-a kJ·molˉ1 ,一定条件下,将2mol X和2 mol Y通入2L的恒容密闭容器中,反应10s,测得生成0.5molZ。下列说法正确的是
A.10s内,X的平均反应速率为0.025 mol·Lˉ1·sˉ1
B.第10s时,Y的反应速率为0.075 mol·Lˉ1·sˉ1
C.第10s时,X为 1.5 mol,Y的浓度为0.25 mol·Lˉ1
D.10s内,X和Y反应放出的热量为a kJ
【答案】C
【解析】
试题分析:X是固体,不能表示反应速率,故A错误; 10s内Y的反应速率为0.075 mol·Lˉ1·sˉ1,是平均速率不是瞬时速率,故B错误;
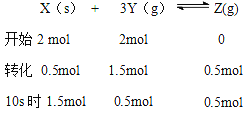
第10s时,X为 1.5 mol,Y的浓度为0.25 mol·Lˉ1,故C正确;
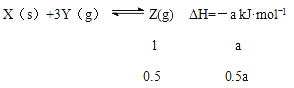
10s内,X和Y反应放出的热量为0.5a kJ,故D错误。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目