题目内容
归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结,归纳正确的是
①常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则有
c (Na+) + c(H+)=c(OH-) + c(CH3COO-)
②对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,生成物的百分含量一定增加
③常温下,AgCl在同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同
④常温下,已知醋酸电离平衡常数为Ka,醋酸根水解平衡常数为Kh,水的离子积为Kw,则有:
Ka∶Kh=Kw
| A.①④ | B.①②④ | C.②③ | D.③④ |
A
解析试题分析:①常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,根据混合液中的电荷守恒知,c (Na+) + c(H+)=c(OH-) + c(CH3COO-),正确;②对已建立化学平衡的某可逆反应,如果通过减小生成物的浓度使化学平衡向正反应方向移动时,生成物的百分含量会减小,错误;③同物质的量浓度的CaCl2和NaCl溶液中,CaCl2溶液中氯离子浓度为NaCl溶液中氯离子浓度的2倍,根据沉淀溶解平衡知识知,常温下,AgCl在CaCl2溶液中的溶解度小于在NaCl溶液中的溶解度,错误;④醋酸电离平衡常数表达式为Ka=c(H+)c(CH3COO-)/c(CH3COOH),醋酸根水解平衡常数表达式为
Kh=c(OH-)c(CH3COOH)/c(CH3COO-),水的离子积为Kw=c(H+)c(OH-),则有:Ka∶Kh=Kw,正确,选A。
考点:考查电解质溶液,涉及弱电解质的电离、沉淀溶解平衡和电解质溶液的电荷守恒式。

对可逆反应N2(g) +3H2(g) 2NH3(g),△H=-92.4 kJ.mol-1下列叙述正确的是
2NH3(g),△H=-92.4 kJ.mol-1下列叙述正确的是
| A.达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大 |
| B.若单位时间内消耗x mol N2,同时生成2x mol NH3,则反应达到平衡状态 |
| C.达到平衡后,将容器体积减小为原来的一半,重新达到平衡后,c(NH3)变为原平衡时的2倍 |
| D.若达到平衡时,共放出46.2kJ热量,则有l mo1NH3(g)生成 |
一定温度下,将1 mol A和1 mol B气体充入2L恒容密闭容器,发生反应A(g)+B(g)  xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确是
xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确是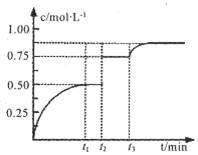
| A.反应方程式中的x=l |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是移去少量物质D |
| D.t1~t3间该反应的平衡常数均为4 |
反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率可表示为
4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率可表示为
A. (NH3)=0.010 0 mol/(L·s) (NH3)=0.010 0 mol/(L·s) |
B. (O2)=0.001 0 mol/(L·s) (O2)=0.001 0 mol/(L·s) |
C. (NO)=0.001 0 mol/(L·s) (NO)=0.001 0 mol/(L·s) |
D. (H2O)=0.045 mol/(L·s) (H2O)=0.045 mol/(L·s) |
可逆反应2SO2+O2 2SO3,正反应速率分别用v(SO2)、v(O2)、v(SO3)(mol·L-1·min-1)表示,逆反应速率分别用v′(SO2)、v′(O2)、v′(SO3)(mol·L-1·min-1)表示,当反应达到化学平衡时,正确的关系是
2SO3,正反应速率分别用v(SO2)、v(O2)、v(SO3)(mol·L-1·min-1)表示,逆反应速率分别用v′(SO2)、v′(O2)、v′(SO3)(mol·L-1·min-1)表示,当反应达到化学平衡时,正确的关系是
①v(SO2)=v′(SO2)
②v(O2)=v′(SO2)=v(SO3)
③v(O2)= v′(SO2)
v′(SO2)
④v′(SO2)=v′(O2)=v′(SO3)
| A.①②③④ | B.①②③ | C.②③④ | D.①③ |
在一定温度下,某容积可变的密闭容器中,建立下列化学平衡:C(s)+H2O(g)  CO(g)+H2(g)。下列叙述中不能说明上述可逆反应已达到化学平衡状态的是( )。
CO(g)+H2(g)。下列叙述中不能说明上述可逆反应已达到化学平衡状态的是( )。
| A.体系的压强不再发生变化 |
| B.v正(CO)=v逆(H2O) |
| C.生成n mol CO的同时生成n mol H2 |
| D.1 mol H—H键断裂的同时断裂2 mol H—O键 |
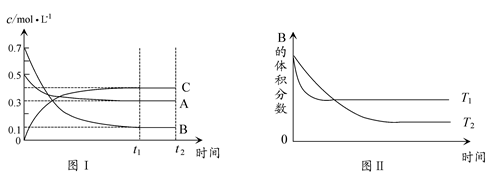
 2C(g) ΔH>0
2C(g) ΔH>0 2C(g)
2C(g)