题目内容
A是一种重要的化工原料,其产量可以用来衡量一个国家的石油化工水平,C是一种酸性物质,D是具有果香气味的烃的衍生物.A、B、C、D在一定条件下存在如下转化关系(石蜡油含17个碳原子以上的液态烷烃,部分反应条件、产物被省略).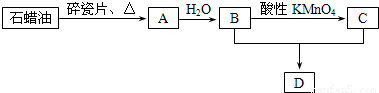
(1)工业上,由石油获得汽油、煤油、石蜡油等成份的方法是 .
(2)A→B的反应类型是 ;B+C→D的反应类型是 .
(3)有机反应中,条件不同往往反应产物也不同.题中B转化为C时,B发生了氧化反应,请写出已学过的B在一定条件下发生氧化反应,转化为另一种烃的衍生物的化学方程式 .
(4)写出B+C转化为D 的化学方程式 .
实验室常用如图所示装置制取D,请在图所示方框中补充画出有关仪器,并标明所盛药品的名称.
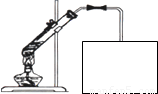
(5)丁烷和戊烷等烷烃是石蜡油获得A的过程中的中间产物.
①请写出丁烷的所有同分异构体的结构简式 .
②戊烷的一种同分异构体,它的一氯取代物有4种,则这种同分异构体的结构简式为 .
【答案】分析:A是一种重要的化工原料,其产量可以用来衡量一个国家的石油化工水平,A为C2H4,乙烯与水发生加成反应生成B,B为乙醇,乙醇在酸性高锰酸钾条件下生成C,C是一种酸性物质,且B与C生成D,D是具有果香气味的烃的衍生物,故C为乙酸,D为乙酸乙酯,据此解答.
解答:解:A是一种重要的化工原料,其产量可以用来衡量一个国家的石油化工水平,A为C2H4,乙烯与水发生加成反应生成B,B为乙醇,乙醇在酸性高锰酸钾条件下生成C,C是一种酸性物质,且B与C生成D,D是具有果香气味的烃的衍生物,故C为乙酸,D为乙酸乙酯,
(1)工业上,由石油获得汽油、煤油、石蜡油等成份的方法是蒸馏,
故答案为:蒸馏;
(2)A→B是烯与水发生加成反应生成乙醇,
B+C→D是乙酸与乙醇发生酯化反应生成乙酸乙酯,
故答案为:加成反应,酯化反应;
(3)乙醇在铜作催化剂、加热条件下可以氧化物乙醛,反应方程式为:2CH3CH2OH+O2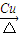 2CH3CHO+2H2O,
2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2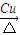 2CH3CHO+2H2O;
2CH3CHO+2H2O;
(4)乙酸与乙醇发生酯化反应生成乙酸乙酯的化学方程式为:CH3COOH+CH3CH2OH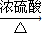 CH3COOCH2CH3+H2O,实验室制取乙酸乙酯,用饱和的碳酸钠溶液接受蒸馏出的乙酸乙酯,便于分层、同时除去乙酸与乙醇,故缺少的装置为
CH3COOCH2CH3+H2O,实验室制取乙酸乙酯,用饱和的碳酸钠溶液接受蒸馏出的乙酸乙酯,便于分层、同时除去乙酸与乙醇,故缺少的装置为
故答案为:CH3COOH+CH3CH2OH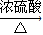 CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,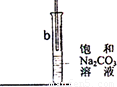 ;
;
(5)①丁烷的所有同分异构体的结构简式为:CH3-CH2-CH2-CH3、(CH3)3CH,
故答案为:CH3-CH2-CH2-CH3、(CH3)3CH;
②戊烷的一种同分异构体,它的一氯取代物有4种,则这种同分异构体的结构简式为:(CH3)2CHCH2CH3,
故答案为:(CH3)2CHCH2CH3.
点评:本题考查有机推断、乙酸乙酯的制备等,涉及烯、醇、醛、羧酸的性质以及同分异构体的书写等,是对有机化合物知识的综合考查,难度中等,注意基础知识的掌握.
解答:解:A是一种重要的化工原料,其产量可以用来衡量一个国家的石油化工水平,A为C2H4,乙烯与水发生加成反应生成B,B为乙醇,乙醇在酸性高锰酸钾条件下生成C,C是一种酸性物质,且B与C生成D,D是具有果香气味的烃的衍生物,故C为乙酸,D为乙酸乙酯,
(1)工业上,由石油获得汽油、煤油、石蜡油等成份的方法是蒸馏,
故答案为:蒸馏;
(2)A→B是烯与水发生加成反应生成乙醇,
B+C→D是乙酸与乙醇发生酯化反应生成乙酸乙酯,
故答案为:加成反应,酯化反应;
(3)乙醇在铜作催化剂、加热条件下可以氧化物乙醛,反应方程式为:2CH3CH2OH+O2
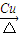 2CH3CHO+2H2O,
2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2
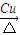 2CH3CHO+2H2O;
2CH3CHO+2H2O;(4)乙酸与乙醇发生酯化反应生成乙酸乙酯的化学方程式为:CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O,实验室制取乙酸乙酯,用饱和的碳酸钠溶液接受蒸馏出的乙酸乙酯,便于分层、同时除去乙酸与乙醇,故缺少的装置为
CH3COOCH2CH3+H2O,实验室制取乙酸乙酯,用饱和的碳酸钠溶液接受蒸馏出的乙酸乙酯,便于分层、同时除去乙酸与乙醇,故缺少的装置为
故答案为:CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O, ;
;(5)①丁烷的所有同分异构体的结构简式为:CH3-CH2-CH2-CH3、(CH3)3CH,
故答案为:CH3-CH2-CH2-CH3、(CH3)3CH;
②戊烷的一种同分异构体,它的一氯取代物有4种,则这种同分异构体的结构简式为:(CH3)2CHCH2CH3,
故答案为:(CH3)2CHCH2CH3.
点评:本题考查有机推断、乙酸乙酯的制备等,涉及烯、醇、醛、羧酸的性质以及同分异构体的书写等,是对有机化合物知识的综合考查,难度中等,注意基础知识的掌握.

练习册系列答案
相关题目

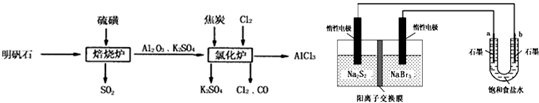
 化工原科,在工农业生产中有广泛的用途。右图是实验室中制取干燥氨气的简易装置。根据此装置回答下列问题:
化工原科,在工农业生产中有广泛的用途。右图是实验室中制取干燥氨气的简易装置。根据此装置回答下列问题: