题目内容
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图: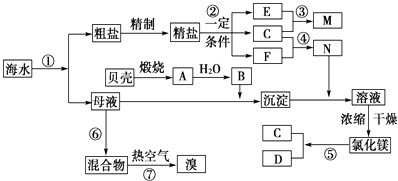
(1)Ⅰ.①写出N的化学式;②写出反应②的化学方程式 .
(2)Ⅱ.粗盐中含有Ca2+、Mg2+、SO42﹣等杂质,精制时所用的试剂为:①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,以上试剂添加的顺序可以为 .
A.②③④①
B.③④②①
C.④③②①
D.③②④①
(3)Ⅲ.提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2 . ①若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是 .
A.分解反应 B.化合反应C.置换反应 D.复分解反应
②若用来提取Br2 , 反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是 .
A.从外地购买 B.在当地新建生产厂
C.从本厂生产烧碱处循环 D.从本厂生产镁单质处循环
③母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2乙:母液先提取Br2 , 后提取Mg
请你判断哪个更合适?(填“甲”或“乙),理由是 .
【答案】
(1)HCl;2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(2)AD
(3)C;CD;乙;若先提取镁,海水中会残留大量氢氧化钙,再用氯气提取溴单质时会损耗大量氯气
【解析】解:(1)Ⅰ.①根据流程图知:反应2为精盐溶液的电解,反应物是氯化钠和水,产物是氯气、氢气、氢氧化钠,C+F→N,N能溶解沉淀,C既能和F反应又能和E反应,所以,E为NaOH,F为H2 , C为Cl2 , N为HCl,所以答案是:HCl;②电解食盐水时,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,同时生成氢氧化钠,方程式为2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑,所以答案是:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,所以答案是:2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑;(2)Ⅱ.SO
2NaOH+H2↑+Cl2↑;(2)Ⅱ.SO ![]() 、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,盐酸能除去过量的Na2CO3溶液和NaOH溶液,所以应先加BaCl2溶液再加Na2CO3溶液,最后加入盐酸,试剂添加的顺序可以为②③④①或③②④①,所以答案是:AD;(3)Ⅲ.①液和B反应为海水中的镁离子和氢氧化钙反应,为复分解反应,得到氢氧化镁的沉淀,制取盐酸为化合反应,氢氧化镁和盐酸反应得到氯化镁,为复分解反应,氯化镁电解为分解反应,该过程中未涉及的反应为置换反应,所以答案是:C;②提取Br2 , 反应⑥所用的气态氧化剂为氯气,本厂生产烧碱为电解氯化钠溶液,产物中有氯气,本厂生产镁单质,是电解无水氯化镁,电解氯化镁的产物为镁和氯气,所以答案是:CD;③母液用来提取Mg和Br2 , 若先提取镁,海水中会残留大量Ca(OH)2 , Ca(OH)2能和氯气反应生成氯化钙和次氯酸钙和水,再用Cl2提取溴时会消耗大量Cl2 , 所以乙观点合理,所以答案是:乙;若先提取镁,海水中会残留大量Ca(OH)2 , 再用Cl2提取溴时会消耗大量Cl2 .
、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,盐酸能除去过量的Na2CO3溶液和NaOH溶液,所以应先加BaCl2溶液再加Na2CO3溶液,最后加入盐酸,试剂添加的顺序可以为②③④①或③②④①,所以答案是:AD;(3)Ⅲ.①液和B反应为海水中的镁离子和氢氧化钙反应,为复分解反应,得到氢氧化镁的沉淀,制取盐酸为化合反应,氢氧化镁和盐酸反应得到氯化镁,为复分解反应,氯化镁电解为分解反应,该过程中未涉及的反应为置换反应,所以答案是:C;②提取Br2 , 反应⑥所用的气态氧化剂为氯气,本厂生产烧碱为电解氯化钠溶液,产物中有氯气,本厂生产镁单质,是电解无水氯化镁,电解氯化镁的产物为镁和氯气,所以答案是:CD;③母液用来提取Mg和Br2 , 若先提取镁,海水中会残留大量Ca(OH)2 , Ca(OH)2能和氯气反应生成氯化钙和次氯酸钙和水,再用Cl2提取溴时会消耗大量Cl2 , 所以乙观点合理,所以答案是:乙;若先提取镁,海水中会残留大量Ca(OH)2 , 再用Cl2提取溴时会消耗大量Cl2 .