题目内容
【题目】溶洞中溶有碳酸氢钙的水,当从洞顶向洞底滴落时,水分的蒸发、压强的减小及温度的升高都会析出碳酸钙沉淀。下列实验不能实现碳酸氢钙转化为碳酸钙的是( )
A. B.
B. C.
C.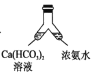 D.
D.
【答案】B
【解析】
A. 浓硫酸能够吸水,促进碳酸氢钙溶液中水分蒸发,溶液中会析出碳酸钙沉淀,能实现碳酸氢钙转化为碳酸钙,故A正确;
B. 浓硝酸不能吸水,不能促进碳酸氢钙溶液中水分蒸发,溶液中不会析出碳酸钙沉淀,不能实现碳酸氢钙转化为碳酸钙,故B错误;
C. 浓氨水不断挥发出NH3,溶解在碳酸氢钙溶液中呈碱性,保证碳酸氢钙溶液中没有酸性物质,防止部分碳酸氢钙不转化,能实现碳酸氢钙转化为碳酸钙,故C正确;
D. 碳酸氢钙加热,温度升高会析出碳酸钙沉淀,能实现碳酸氢钙转化为碳酸钙,故D正确;
题目要求选不能实现的,故选B。

练习册系列答案
相关题目