题目内容
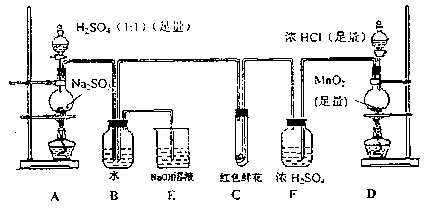
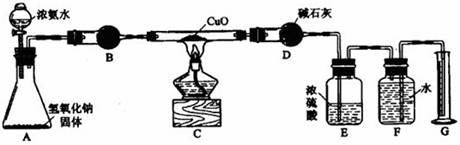
(14分)氨气与灼热的氧化铜反应生成铜、氮气和水。利用下图所示实验装置可测定氨分子的组成(图中夹持、固定装置均略去)。回答下列问题。
⑴写出氨气与氧化铜反应的化学方程式。
⑵在A的锥形瓶中放入NaOH固体的目的是。
⑶在干燥管B里不能选用的干燥剂是(填序号)。
A 碱石灰 B 生石灰 C 五氧化二磷 D 氢氧化钠
⑷在C的玻管中观察到的现象是 。
⑸E装置中盛装浓硫酸的目的是 。
⑹待实验完毕后,若实验测得N2的体积(折算成标准状况)为aL,则被还原的氧化铜的物质的量为 mol;若测得干燥管D增重bg,则氨分子中氮、氢的原子个数比为 。(用含a、b字母的代数式表示)

⑴写出氨气与氧化铜反应的化学方程式。
⑵在A的锥形瓶中放入NaOH固体的目的是。
⑶在干燥管B里不能选用的干燥剂是(填序号)。
A 碱石灰 B 生石灰 C 五氧化二磷 D 氢氧化钠
⑷在C的玻管中观察到的现象是 。
⑸E装置中盛装浓硫酸的目的是 。
⑹待实验完毕后,若实验测得N2的体积(折算成标准状况)为aL,则被还原的氧化铜的物质的量为 mol;若测得干燥管D增重bg,则氨分子中氮、氢的原子个数比为 。(用含a、b字母的代数式表示)
⑴2NH3+3CuO N2+3Cu+3H2O (2分)
N2+3Cu+3H2O (2分)
⑵NaOH固体吸水及溶解产生的热利于氨气的逸出。(2分)
⑶C (2分)
⑷黑色粉末变为光亮的红色固体。(2分)
⑸将反应剩余的氨吸收,防止F中的水蒸气进入D中,引起测量误差。(2分)
⑹3a/22.4(2分) 9a/11.2b(2分)
 N2+3Cu+3H2O (2分)
N2+3Cu+3H2O (2分)⑵NaOH固体吸水及溶解产生的热利于氨气的逸出。(2分)
⑶C (2分)
⑷黑色粉末变为光亮的红色固体。(2分)
⑸将反应剩余的氨吸收,防止F中的水蒸气进入D中,引起测量误差。(2分)
⑹3a/22.4(2分) 9a/11.2b(2分)
考查氨气的制取与性质、分子组成的测定;
实验目的之一是测定氨分子的组成,结合所给装置可看出,通过氨气还原氧化铜,氮元素转化为氮气,可用排水法来测定其体积,而氢元素转化为水,其质量可通过装置D的增重来测得。
(1)氨气中的氮元素为其最低负价,可将氧化铜还原:2NH3+3CuO N2+3Cu+3H2O
N2+3Cu+3H2O
(2)此为简易法来制备氨气;在氨水中存在平衡:NH4++OH- NH3·H2O
NH3·H2O NH3+H2O
NH3+H2O
NaOH固体溶解产生大量的热且可产生大量的OH-,均可促使氨气的生成与逸出:NH3·H2O NH3↑+H2O
NH3↑+H2O
(3)氨所碱性氧化,不能用酸性干燥剂来干燥,故答案为C
(4)氧化铜为黑色粉末,被氨气还原为红色的金属铜
(5)为保证装置D只吸收反应所生成的水,可知装置E主要有两个作用,一是吸收未反应的氨气,二是防止装置F中的水气进入装置E中
(6)氨气的物质的量为a/22.4 mol,由化学方程式可知,被还原的氧化铜的物质的量为3a/22.4 mol;
水的物质的量为b/18 mol;所以氨分子中氮、氢的原子个数比为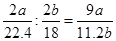
实验目的之一是测定氨分子的组成,结合所给装置可看出,通过氨气还原氧化铜,氮元素转化为氮气,可用排水法来测定其体积,而氢元素转化为水,其质量可通过装置D的增重来测得。
(1)氨气中的氮元素为其最低负价,可将氧化铜还原:2NH3+3CuO
 N2+3Cu+3H2O
N2+3Cu+3H2O(2)此为简易法来制备氨气;在氨水中存在平衡:NH4++OH-
 NH3·H2O
NH3·H2O NH3+H2O
NH3+H2ONaOH固体溶解产生大量的热且可产生大量的OH-,均可促使氨气的生成与逸出:NH3·H2O
 NH3↑+H2O
NH3↑+H2O(3)氨所碱性氧化,不能用酸性干燥剂来干燥,故答案为C
(4)氧化铜为黑色粉末,被氨气还原为红色的金属铜
(5)为保证装置D只吸收反应所生成的水,可知装置E主要有两个作用,一是吸收未反应的氨气,二是防止装置F中的水气进入装置E中
(6)氨气的物质的量为a/22.4 mol,由化学方程式可知,被还原的氧化铜的物质的量为3a/22.4 mol;
水的物质的量为b/18 mol;所以氨分子中氮、氢的原子个数比为
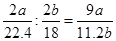

练习册系列答案
 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目