题目内容
【题目】某校化学实验兴趣小组为了验证在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略)。
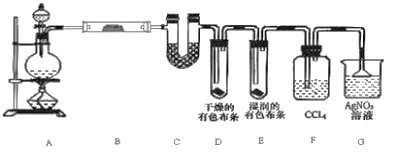
请按要求回答下列问题:
(1)写出烧瓶中发生反应的离子方程式_______________________________。
(2)①装置B中盛放的试剂名称是____________,作用是___________,现象是______________;
②装置D和E出现的不同现象说明的问题是__________________________________;
③写出G中发生反应的离子方程式____________________________。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出应该在装置
___________之间(填装置字母序号)增加一个装置,所增加装置里面的试剂可以为_______(填字母序号)
a. 湿润的碘化钾淀粉试纸 b. 浓硫酸
c. 湿润的红色布条 d. 饱和食盐水
(4)A装置中分液漏斗内所用溶液浓度为12 mol/L,现欲用其配制100 mL 2 mol/L的稀溶液。则需量取________ mL浓溶液,量取所用量筒的规格是________(选填“10mL”、“25mL”或“50mL”)。若所配制的稀溶液浓度偏大,则下列可能的原因分析中正确的是__________
a. 配制前,容量瓶中有少量蒸馏水 b. 量取浓溶液时,仰视液面
c. 未经冷却,立即转移至容量瓶定容 d. 定容时,仰视液面
【答案】 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 无水硫酸铜 验证有水蒸气挥发出来 固体由白色变为蓝色 干燥的氯气无漂白性,次氯酸有漂白性 Ag++Cl-=AgCl↓ F G ac 16.7 25mL b c
Mn2++Cl2↑+2H2O 无水硫酸铜 验证有水蒸气挥发出来 固体由白色变为蓝色 干燥的氯气无漂白性,次氯酸有漂白性 Ag++Cl-=AgCl↓ F G ac 16.7 25mL b c
【解析】本题主要考查对于“验证在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质”实验的评价。
(1)烧瓶中发生反应的离子方程式:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。
(2)①装置B中盛放的试剂名称是无水硫酸铜,作用是验证有水蒸气挥发出来,现象是固体由白色变为蓝色;
②装置D和E出现的不同现象说明的问题是干燥的氯气无漂白性,次氯酸有漂白性;
③G中发生反应的离子方程式:Ag++Cl-=AgCl↓ 。
(3)为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出应该在装置FG之间增加一个装置,验证没有氯气存在,所增加装置里面的试剂可以为ac。
(4)c浓V浓= c稀V稀,V浓=c稀V稀/c浓=2×100/12mL=16.7mL,则需量取16.7mL浓溶液,量取所用量筒的规格是25mL。若所配制的稀溶液浓度偏大,则下列可能的原因分析中正确的是bc。因为a. 不影响结果;b. 量取浓溶液体积增大,所配制的稀溶液浓度偏大;c. 溶液体积减小,所配制的稀溶液浓度偏大;d. 所配制的稀溶液体积增大,所配制的稀溶液浓度偏小。故选bc。

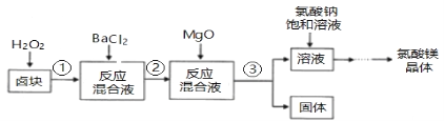
【题目】锰酸锂(LiMn2O4)可作为锂离子电池的正极材料.工业上利用软锰矿浆吸收含硫烟气(SO2 和O2)制备锰酸锂,生产流程如图1: 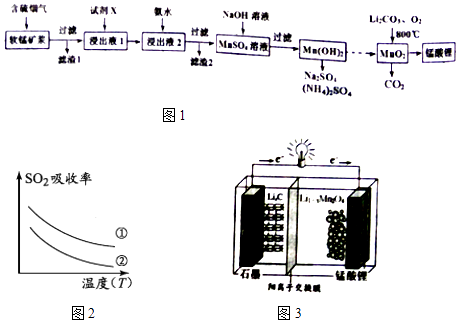
已知:①软锰矿主要成分为MnO2 , 含少量Fe2O3、FeO、Al2O3、SiO2等杂质.
②软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强.
③部分氢氧化物沉淀相关的溶液pH如表一:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
(1)已知:(图2)表二 表二
实验序号 | SO2浓度(gm﹣3) | 烟气流速(mLmin﹣1) |
① | 4.1 | 55 |
② | 4.1 | 96 |
下列措施可提高SO2吸收率的是(填序号)
a.降低通入含硫烟气的温度 b.升高通入含硫烟气的温度
c.减少软锰矿浆的进入量 d.减小通入含硫烟气的流速
(2)加入试剂X能提高产品纯度,则X可以是(填化学式)
(3)加氨水调溶液pH在5~6之间,目的是 .
(4)锰酸锂可充电电池(图3)的总反应式为:Li1﹣xMnO4+LixC ![]() LiMnO4+C(x<1) ①放电时,电池的正极反应式为
LiMnO4+C(x<1) ①放电时,电池的正极反应式为
②充电时,若转移1mole﹣ , 则石墨电极将增重g.