题目内容
在100mL含有等物质的量的HBr和H2SO3的溶液中通入0.01mol Cl2,有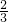 的Br -转变为Br2(已知Br2能氧化H2SO3).则原溶液中HBr和H2SO3的物质的量浓度为
的Br -转变为Br2(已知Br2能氧化H2SO3).则原溶液中HBr和H2SO3的物质的量浓度为
- A.0.0075 mol?L-1
- B.0.075 mol?L-1
- C.0.008 mol?L-1
- D.0.08 mol?L-1
分析:Br2能氧化H2SO3,则还原性H2SO3>Br-,氯气首先氧化H2SO3为H2SO4,H2SO3反应完毕,然后再氧化Br-,由于Br-部分转变Br2,所以HBr部分被氧化,H2SO3全部被氧化,令原溶液中HBr和H2SO3的浓度为cmol/L,根据电子转移守恒,列方程计算c的值.
解答:Br2能氧化H2SO3,则还原性H2SO3>Br-,氯气首先氧化H2SO3为H2SO4,H2SO3反应完毕,然后再氧化Br-,由于2/3的Br-转变Br2,所以有2/3HBr部分被氧化,H2SO3全部被氧化,令原溶液中HBr和H2SO3的浓度为cmol/L,根据电子转移守恒,则:
0.1L×cmol/L×(6-4)+0.1L×cmol/L×
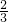 ×1=0.01mol×2,
×1=0.01mol×2,解得:c=0.075,
故选B.
点评:本题考查氧化还原反应计算,难度中等,根据Br2能氧化H2SO3 判断还原性H2SO3>Br-是关键.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(14分)
现有A、B、C、D、E五种强电解质,分别含有下列阴阳离子(离子不可重复)。
| 阴离子 |
|
| 阳离子 |
|
已知:①A、B两溶液呈碱性,C、D、E溶液呈酸性。
②A、E两溶液反应既有气体,又有沉淀生成,A、C两溶液反应只有气体产生。
③D与其他四种溶液反应,均产生沉淀,C只与D反应产生沉淀。
试回答下列问题:
(1)写出:①B的化学式 ,②D与A反应生成难溶物的![]() 表达式 。
表达式 。
(2)A与E在溶液中反应的离子方程式为 。
(3)将pH相同的等体积A、B两种溶液稀释相同倍数后,溶液的pH关系是:![]()
![]() (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)将C溶液逐滴加入到等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为 。
(5)在100mL 0.1![]() E溶液中,逐渐中入35 mL 2
E溶液中,逐渐中入35 mL 2![]()
![]() 溶液,最终得到沉淀的物质的量为 mol。
溶液,最终得到沉淀的物质的量为 mol。
(14分)
现有A、B、C、D、E五种强电解质,分别含有下列阴阳离子(离子不可重复)。
|
阴离子 |
|
|
阳离子 |
|
已知:①A、B两溶液呈碱性,C、D、E溶液呈酸性。
②A、E两溶液反应既有气体,又有沉淀生成,A、C两溶液反应只有气体产生。
③D与其他四种溶液反应,均产生沉淀,C只与D反应产生沉淀。
试回答下列问题:
(1)写出:①B的化学式
,②D与A反应生成难溶物的 表达式
。
表达式
。
(2)A与E在溶液中反应的离子方程式为 。
(3)将pH相同的等体积A、B两种溶液稀释相同倍数后,溶液的pH关系是:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)将C溶液逐滴加入到等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为 。
(5)在100mL 0.1
 E溶液中,逐渐中入35 mL 2
E溶液中,逐渐中入35 mL 2
 溶液,最终得到沉淀的物质的量为 mol。
溶液,最终得到沉淀的物质的量为 mol。
 Cr2O72-+H2O
Cr2O72-+H2O
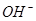 、
、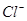 、
、 、
、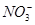 、
、
 、
、 、
、 、
、 、
、