��Ŀ����
������̼�������洢��ת���ǵ���ѧ�о����ȵ�����֮һ��
(1)���ɵ��������������һ�������¿�ֱ�ӹ���ֽ�CO2��������Ӧ��2CO2(g)=2CO(g)��O2(g)���÷�Ӧ�Ħ�H 0����S 0(ѡ�����������������)���ڵ����£��÷�Ӧ (��ܡ����ܡ�)�Է����С�
(2)CO2ת��;��֮һ������̫���ܻ��������ֽܷ�ˮ��H2��Ȼ��H2��CO2ת��Ϊ�״���������ѧƷ������Ϊ�÷�����Ҫ����ļ��������� ��
a�������������
b���������ȡ�������ӷ�Ӧ��ϵ����Ч���룬����CO2������ת��
c��������̼��ˮ��Դ�Ĺ�Ӧ
(1)�����������ܡ�(2)ab
����

2013��9�£��й��������е������������ص������������������ӱ������ϵȵصĿ�����Ⱦ��Ϊ6��������Ⱦ�������ض���Ⱦ������β����ȼú����������ȡů�ŷŵ�CO2�ȶ��������γɵ�ԭ��
��1������β����������Ҫԭ��Ϊ;2NO(g)��2CO(g) N2��g)��2CO2��g)�� ��H��0����һ���¶��£���һ����̶����ܱ������г���һ������NO��CO��t1ʱ�̴ﵽƽ��״̬��
N2��g)��2CO2��g)�� ��H��0����һ���¶��£���һ����̶����ܱ������г���һ������NO��CO��t1ʱ�̴ﵽƽ��״̬��
�����жϸ÷�Ӧ�ﵽƽ��״̬�ı�־�ǣߣߣߣߡ�
| A���ڵ�λʱ��������1mol CO2��ͬʱ������lmol CO |
| B�����������ܶȲ��ٸı� |
| C����������ƽ����Է����������ٸı� |
| D����������ѹǿ���ٱ仯 |

����Ҫͬʱ��߸÷�Ӧ�����ʺ�NO��ת���ʣ���ȡ�Ĵ�ʩ��_____��____����д��2����
(2���ı�ú�����÷�ʽ�ɼ��ٻ�����Ⱦ��ͨ���ɽ�ˮ����ͨ�����ȵ�̼�õ�ˮú�����䷴Ӧԭ��ΪC(s)��H2O(g)
 CO(g)��H2(g) ��H��+131.3kJ/mol��
CO(g)��H2(g) ��H��+131.3kJ/mol���ٸ÷�Ӧ��___�����Է����У�����¡����¡�����
��ú���������в������к�����H2S����������Na2C03��Һ���գ��÷�Ӧ�����ӷ���ʽΪ____������֪��H2S�� Ka1��9.1��10-8��Ka2��1.1��10-12��H2CO3��Ka1��4.30��10-7��Ka2��5.61��10-11��
(3����֪��Ӧ��CO(g����H2O��g��
 CO2��g����H2��g�����ֽ���ͬ����CO��g����H2O��g���ֱ�ͨ�˵����Ϊ2L�ĺ����ܱ������н��з�Ӧ���õ������������ݣ�
CO2��g����H2��g�����ֽ���ͬ����CO��g����H2O��g���ֱ�ͨ�˵����Ϊ2L�ĺ����ܱ������н��з�Ӧ���õ������������ݣ�| ʵ�� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | ��ƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
��ʵ��1������ƽ�ⳣ��K��______������С������λ����
��ʵ��3�У���ƽ��ʱ��CO��ת���ʴ���ˮ��������a��b��������Ĺ�ϵ��______��
�۸÷�Ӧ�ġ�H ______0(�����������������9000Cʱ������һ��ʵ�飬�ڴ������м���l0mol CO,5mo1 H2O,2mo1 CO2,5mol H2�����ʱ����______�������������������������������
�״�����Ҫ�Ļ�ѧ��ҵ����ԭ�Ϻ�Һ��ȼ�ϡ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�״��Ʊ����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧ��Ӧƽ�ⳣ�����±���ʾ��
| ��ѧ��Ӧ | ƽ�ⳣ�� | �¶ȣ��棩 | |
| 500 | 800 | ||
��2H2(g)+CO(g)  CH3OH(g) CH3OH(g) | K1 | 2��5 | 0��15 |
��H2(g)+CO2(g)  H2O (g)+CO(g) H2O (g)+CO(g) | K2 | 1��0 | 2��50 |
��3H2(g)+ CO2(g)  CH3OH(g)+H2O (g) CH3OH(g)+H2O (g) | K3 | | |
��1����Ӧ���� ������ȡ����ȡ�����Ӧ��
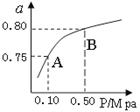
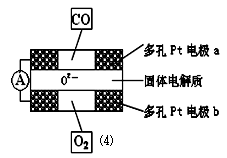
��2��ij�¶��·�Ӧ����H2��ƽ��ת���ʣ�a������ϵ��ѹǿ(P)�Ĺ�ϵ��ͼ��ʾ����ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K(A) K(B)�����������������������
��3���жϷ�Ӧ�ۡ�H 0�� ��S 0���>����=����<�����ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3= ����K1��K2��ʾ������500�桢2L���ܱ������У����з�Ӧ�ۣ����ijʱ��H2��CO2�� CH3OH��H2O�����ʵ����ֱ�Ϊ6mol��2 mol��10 mol��10 mol����ʱv(��) v(��)���>����=����<����
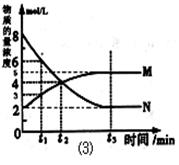
��4��һ���¶��£���3 L�ݻ��ɱ���ܱ������з�����Ӧ�ڣ���֪c(CO)�뷴Ӧʱ��t�仯���ߢ���ͼ��ʾ������t0ʱ�̷ֱ�ı�һ�����������ߢ��Ϊ���ߢ�����ߢ�
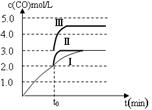
�����ߢ��Ϊ���ߢ�ʱ���ı�������� ��
�����ߢ��Ϊ���ߢ�ʱ���ı�������� ��
��5���״�ȼ�ϵ��ͨ�����ò��缫���乤��ԭ����ͼ��ʾ�������ĵ缫��ӦΪ�� ��
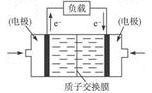
��6��һ�������¼״���һ����̼��Ӧ���Ժϳ����ᡣͨ��״���£���0��2 mol/L�Ĵ�����0��1 mol/LBa(OH)2��Һ�������ϣ�������Һ������Ũ���ɴ�С��˳��Ϊ ��
��������ЧӦ����Դ��ȱ�����⣬��ν��ʹ����е�CO2���������Կ������ã������˸�����ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·�����Ӧ��CO2(g)��3H2(g) CH3OH(g)��H2O(g)���÷�Ӧ�������仯��ͼ��ʾ��
CH3OH(g)��H2O(g)���÷�Ӧ�������仯��ͼ��ʾ��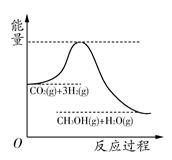
(1)������Ӧƽ�ⳣ��K�ı���ʽΪ________���¶Ƚ��ͣ�ƽ�ⳣ��K________(����������䡱��С��)��
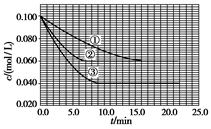
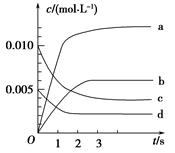
(2)�����Ϊ2 L���ܱ������У�����1 mol CO2��3 mol H2�����CO2�����ʵ�����ʱ��仯���±���ʾ���ӷ�Ӧ��ʼ��5 minĩ��������Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(H2)��________��
| t/min | 0 | 2 | 5 | 10 | 15 |
| n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
(3)����ͬ�¶��ݻ�����������£���˵���÷�Ӧ�Ѵ�ƽ��״̬����________(��д�����ĸ)��
a��n(CO2)��n(H2)��n(CH3OH)��n(H2O)��1��3��1��1
b��������ѹǿ���ֲ���
c��H2������������CH3OH����������֮��Ϊ3��1
d�������ڵ��ܶȱ��ֲ���
(4)����������ʹ������Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����________(��д�����ĸ)��
a����ʱ�����CH3OH����
b���ʵ������¶�
c�������������ݻ����䣬�ٳ���1 mol CO2��3 mol H2
d��ѡ���Ч�Ĵ���
��2 L�ܱ������ڣ�800 ��ʱ��Ӧ2NO(g)��O2(g)  2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
| ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)��ͼ��ʾNO2�ı仯��������________����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v��________��
(2)��˵���÷�Ӧ�Ѵﵽƽ��״̬����________��
a��v(NO2)��2v(O2) b��������ѹǿ���ֲ���
c��v��(NO)��2v��(O2) d���������ܶȱ��ֲ���
(3)Ϊʹ�÷�Ӧ�ķ�Ӧ�����������д�ʩ��ȷ����________��
a����ʱ�����NO2���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч����
 Si3N4 + 6CO���÷�Ӧ�����е������仯��ͼ����ʾ���ش��������⣺
Si3N4 + 6CO���÷�Ӧ�����е������仯��ͼ����ʾ���ش��������⣺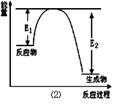
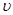 ������
������ 
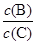 �� (���������С�����䡱)��
�� (���������С�����䡱)�� CH3OCH3(g)��H2O(g) ��H����23.5 kJ��mol��1����T1�棬�����ܱ������н�������ƽ�⣬��ϵ�и����Ũ����ʱ��仯��ͼ��ʾ��
CH3OCH3(g)��H2O(g) ��H����23.5 kJ��mol��1����T1�棬�����ܱ������н�������ƽ�⣬��ϵ�и����Ũ����ʱ��仯��ͼ��ʾ��
 C�ֱ������ֲ�ͬʵ�������½��У����ǵ���ʼŨ�Ⱦ�Ϊc(A)
C�ֱ������ֲ�ͬʵ�������½��У����ǵ���ʼŨ�Ⱦ�Ϊc(A)