题目内容
为了测定铜铁合金中铜的质量分数,在10.00g试样中加入200mL、0.6mol/L的稀硝酸,充分反应后剩余金属7.48g,再向其中加入50mL、0.4mol/L的稀硫酸,充分振荡后剩余金属6.60g。若硝酸的还原产物只有NO,下列说法正确的是
| A.上述测定不能达到实验目的 | B.剩余的7.48g金属为铜 |
| C.共生成NO气体 0.04mol | D.该合金中铜的质量分数为69.2% |
CD
解析试题分析:铁的金属性强于铜的,所以硝酸首先氧化金属铁,第一次反应后金属过量,硝酸不足,说明生成物一定有硝酸亚铁。加入稀硫酸后金属又溶解了7.48g-6.60g=0.88g,硫酸中氢离子的物质的量是0.05L×0.4mol/L×2=0.04mol,则根据方程式3M+2NO3-+8H+=3M2++2NO↑+4H2O可知,NO的物质的量是0.01mol,参加反应的金属的物质的量是(0.04mol÷8)×3=0.015mol,则M的相对原子质量是0.88÷0.015=58.67,这说明溶解的金属是铁和铜,所以剩余的7.84g金属是铁和铜的混合物,因此第一次溶解的金属铁是10.00g-7.48g=2.52g,物质的量是2.52g÷56g/mol=0.045mol,6.60g全部是金属铜。硝酸的物质的量是0.2L×0.6mol/L=0.12mol,根据方程式3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O可知,生成物硝酸亚铁的物质的量是0.045mol,NO的物质的量是0.03mol,因此共放出NO是0.04mol。设第二次消耗金属铁和铜的物质的量分别是x和y,则56x+64y=0.88、2x+2y=0.01×3,解得x=0.01mol、y=0.005mol,所以合金中铜的质量是6.60g+0.005mol×64g/mol=6.92g,所以该合金中铜的质量分数为69.2%,答案选CD。
考点:考查铁、铜与硝酸以及硫酸反应的有关计算

NA为阿伏加德罗常数,下列叙述正确的是
| A.10 g H18 2O含有的中子数为5NA |
| B.1 mol羟基(-OH)含有的电子数为10NA |
| C.1 mol 氯气参加反应时,电子转移数目一定为2NA |
| D.标准状况下,11.2L己烷含有的分子数为0.5NA |
某结晶水合物的化学式为R?nH2O,其相对分子质量为M。25℃时,将a g该晶体溶于b g H2O中恰好形成V mL饱和溶液。下列表达式正确的是
A.饱和溶液物质的量浓度为: 1000 a(M -18n) mol/L 1000 a(M -18n) mol/L |
B.饱和溶液溶质的质量分数为: |
C.25℃时R的溶解度为: g/100 g H2O g/100 g H2O |
D.饱和溶液的密度为: g/mL g/mL |
一定条件下某容器中各微粒在反应前后的变化如图所示,其中●和○代表不同元素的原子。关于此反应说法错误的是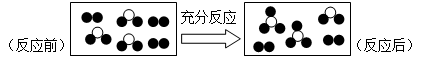
| A.一定属于可逆反应 | B.一定属于化合反应 |
| C.一定属于氧化还原反应 | D.一定属于放热反应 |
阿佛加德罗常数用NA表示,下列叙述正确的是
| A.室温时,1LpH=2的NH4Cl溶液中水电离出10-12molH+ |
| B.常温常压下,46gNO2含3NA个原子 |
| C.1molLiAlH4在125℃完全分解成LiH、H2、Al,转移电子3NA |
| D.12g石墨含有4NA个自由移动的电子 |
下列说法不正确的是(设NA表示阿伏加德罗常数的值)
| A.可用盐析法分离NaCl溶液和淀粉胶体 |
| B.天然油脂的分子中含有酯基,属于酯类 |
| C.T℃时,1 L pH=6的纯水中,含有的OH-数目为l×10-6NA |
| D.12.0 gNaHSO4固体中含有的阳离子数目为0.1 NA |
下列化学用语正确的是( )
A.14C原子结构示意图: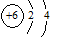 |
B.硝基苯的结构简式: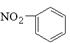 |
C.NH4Cl的电子式: |
| D.FeS2中S的化合价:?2 |
设NA表示阿伏加德罗常数的值。下列叙述不正确的是
| A.1 mol Na2O和Na2O2的混合物中含有的阴、阳离子总数是3NA |
| B.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中含有的氮原子数为0.2NA |
| C.46 g有机物C2H6O中含有的H—O键的数目为NA |
| D.标准状况下,将0.1 mol Cl2通入足量NaOH溶液中,反应转移的电子数为0.1NA |