题目内容
14.在化学反应2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,中下列说法不正确的是( )| A. | 氢元素是还原剂 | B. | O2是氧化剂 | C. | H2发生氧化反应 | D. | O2被还原 |
分析 化学反应2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,H2中的H元素化合价升高为还原剂,被氧化,发生氧化反应;O2中的O元素化合价降低为氧化剂,被还原,发生还原反应,据此分析.
解答 解:A、H2中的H元素化合价升高,则H2为还原剂,故A错误;
B、O2中的O元素化合价降低,则O2为氧化剂,故B正确;
C、H2中的H元素化合价升高,则H2为还原剂,发生氧化反应,故C正确;
D、O2中的O元素化合价降低为氧化剂,被还原,故D正确.
故选:A.
点评 本题主要考查了氧化还原反应的基本概念的判断,比较简单,注意基础知识的积累.

练习册系列答案
相关题目
5.下列说法不正确的是( )
| A. | CO2、SiO2的晶体结构类型不同 | |
| B. | 加热硅、硫晶体使之熔化,克服的作用力不同 | |
| C. | HCl、NaCl溶于水,破坏的化学键类型相同 | |
| D. | NaOH、NH4Cl晶体中既有离子键又有共价键 |
11.由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl-、NH4+、Mg2+、Ba2+、CO32-、SO42-,将该混合物溶于水后得澄清溶液,现取3份各100mL的该溶液分别进行如下实验:
试回答下列问题:
(1)根据实验①对Cl-是否存在的判断是不能确定(填“一定存在”“一定不存在”或“不能确定”),根据实验①②③判断混合物中一定不存在的离子是Ba2+、Mg2+;
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
(3)试确定K+存在(填是或否)存在.
| 实验序号 | 实验内容 | 实验结果 |
| ① | 加AgNO3溶液 | 有白色沉淀生成 |
| ② | 加足量NaOH溶液并加热 | 收集到气体1.12L(标准状况) |
| ③ | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加入足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27g;第二次称量读数为2.33g |
(1)根据实验①对Cl-是否存在的判断是不能确定(填“一定存在”“一定不存在”或“不能确定”),根据实验①②③判断混合物中一定不存在的离子是Ba2+、Mg2+;
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
| 阴离子符号 | 物质的量浓度/mol•L-1 |
9.下列离子方程式书写正确的是( )
| A. | MgSO4溶液与Ba(OH)2溶液反应:SO42-+Ba2+═BaSO4↓ | |
| B. | 向澄清石灰水中加入过量NaHCO3溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| C. | 向Al2(SO4)3溶液中加入过量NaOH溶液:Al3++4OH-═AlO2-+2H2O | |
| D. | 向Ca(ClO2)溶液中通入少量SO2:Ca2++2ClO-+H2O+SO2═CaSO3↓+2HClO |
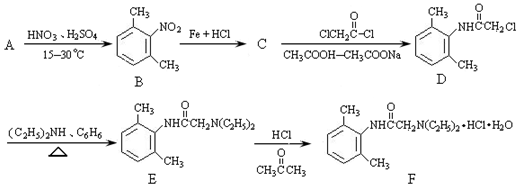
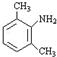 ;
;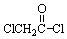 与足量的NaOH溶液共热充分反应的化学方程式:
与足量的NaOH溶液共热充分反应的化学方程式: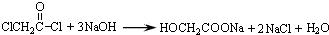 .
.
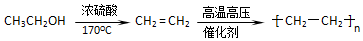

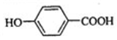 ;
;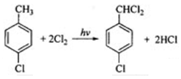 ,该反应类型为取代反应;
,该反应类型为取代反应;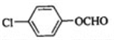 (写结构简式).
(写结构简式).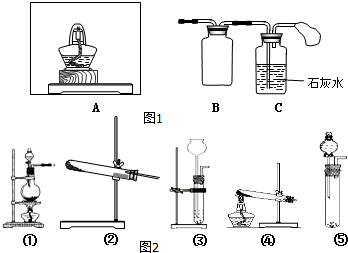 Na2O2是常见的氧化剂,某化学小组的同学欲通过以下实验确定炭粉与Na2O2反应的产物.
Na2O2是常见的氧化剂,某化学小组的同学欲通过以下实验确定炭粉与Na2O2反应的产物.