题目内容
【题目】某温度下,在一密闭容器中发生如下可逆反应:![]() ;
;![]() 若起始时E浓度为a
若起始时E浓度为a![]() ,F、G浓度均为0,达平衡时E浓度为0.5a
,F、G浓度均为0,达平衡时E浓度为0.5a![]() ;若E的起始浓度改为2a
;若E的起始浓度改为2a![]() ,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
A.升高温度时,正反应速率加快、逆反应速率减慢
B.若![]() ,容器体积保持不变,新平衡下E的体积分数为
,容器体积保持不变,新平衡下E的体积分数为![]()
C.若![]() ,容器体积保持不变,新平衡下F的平衡浓度小于
,容器体积保持不变,新平衡下F的平衡浓度小于![]()
![]()
D.若![]() ,容器压强保持不变,新平衡下E的物质的量为amol
,容器压强保持不变,新平衡下E的物质的量为amol
【答案】B
【解析】
A、升高温度正、逆反应速率都增大;
B、容器体积保持不变,![]() ,反应前后气体的物质的量不变,若E的起始浓度改为2a
,反应前后气体的物质的量不变,若E的起始浓度改为2a![]() ,等效为增大压强,平衡不移动,新平衡下E的体积分数与原平衡相等;
,等效为增大压强,平衡不移动,新平衡下E的体积分数与原平衡相等;
C、容器体积保持不变,若E的起始浓度改为2a![]() ,等效为在原平衡的基础上增大E的浓度,反应向正反应进行,F的浓度增大;
,等效为在原平衡的基础上增大E的浓度,反应向正反应进行,F的浓度增大;
D、题目中为物质的量的浓度,不能确定物质具体物质的量.
A、升高温度正、逆反应速率都增大,故A错误;
B、容器体积保持不变,![]() ,反应前后气体的物质的量不变,若E的起始浓度改为2a
,反应前后气体的物质的量不变,若E的起始浓度改为2a![]() ,等效为增大压强,平衡不移动,平衡时E的转化率不变,新平衡下E的体积分数与原平衡相等为
,等效为增大压强,平衡不移动,平衡时E的转化率不变,新平衡下E的体积分数与原平衡相等为![]() ,故B正确;
,故B正确;
C、原平衡时E浓度为0.5a![]() ,
,![]() mol/L-0.5amol/L=0.5a
mol/L-0.5amol/L=0.5a![]() ,故平衡时F的浓度为0.5a
,故平衡时F的浓度为0.5a![]() ,容器体积保持不变,若E的起始浓度改为2a
,容器体积保持不变,若E的起始浓度改为2a![]() ,等效为在原平衡的基础上增大E的浓度,反应向正反应进行,F的浓度增大,故大于0.5a
,等效为在原平衡的基础上增大E的浓度,反应向正反应进行,F的浓度增大,故大于0.5a![]() ,故C错误;
,故C错误;
D、容器压强保持不变,若E的起始浓度改为2a![]() ,与原平衡为等效平衡,E的转化率相同,平衡时E的物质的量为原平衡的2倍,题目中为物质的量的浓度,不能确定物质的量,原平衡E的物质的量不一定是
,与原平衡为等效平衡,E的转化率相同,平衡时E的物质的量为原平衡的2倍,题目中为物质的量的浓度,不能确定物质的量,原平衡E的物质的量不一定是![]() ,故D错误;
,故D错误;
故选B。

 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案【题目】在一定温度下,将气体X和气体Y各![]() 充入10L恒容密闭容器中,发生反应
充入10L恒容密闭容器中,发生反应![]() ,一段时间后达到平衡,反应过程中测定的数据如下表:下列说法正确的是
,一段时间后达到平衡,反应过程中测定的数据如下表:下列说法正确的是![]()
| 2 | 4 | 7 | 9 |
|
|
|
|
|
A.8min时,其他条件不变,若增大X的浓度,则反应速率加快,活化分子百分数增加
B.该温度下此反应的平衡常数![]()
C.其他条件不变,降低温度,反应达到新平衡前![]() 逆
逆![]() 正
正![]()
D.其他条件不变,再充入![]() ,平衡时X的体积分数增大
,平衡时X的体积分数增大
【题目】碱式氯化镁(MgOHCl)常用作塑料添加剂,工业上制备方法较多,其中利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁的工艺属于我国首创。某中学科研小组根据该原理设计如下装置图进行相关实验,装置C中CuO的质量为8.0g。
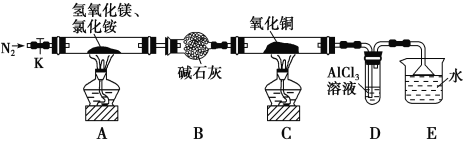
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为:______________。
(2)装置D中生成沉淀,发生反应的离子方程式为___________________。
(3)反应过程中持续通入N2的作用有两点:一是:将装置A中产生的氨气完全导出,二是:_______________________。
(4)反应完毕,装置C中的氧化铜全部由黑色变为红色,称其质量为6.8g,且生成的气体可直接排放到大气中,该反应中转移电子的物质的量为_______mol。
(5)请你设计一个实验方案证明装置C中的氧化铜反应完全后得到的红色固体中含有氧化亚铜。已知:①Cu2O+2H+=Cu2++Cu+H2O
②限选试剂:2 mol·L-1H2SO4溶液、浓硫酸、2 mol·L-1HNO3溶液、10 mol·L-1 HNO3溶液
实验步骤 | 预期现象和结论 |
步骤1:取反应后装置C中的少许固体于试管中 | |
步骤2:______________________________ | _____________________ |