题目内容
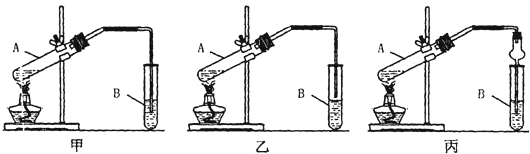
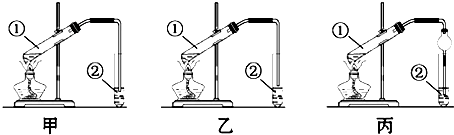
下列实验室中分离或除杂质的方法中不正确的是( )A.用升华法分离碘和碘化钠固体混合物
B.用加热法除去氯化钙中混有的氯化铵
C.用蒸馏法分离乙醇和丁醇混合物
D.用萃取法除去溴苯中混有的溴单质
解析:选项A碘单质易升华,可与NaI分离;选项B,NH4Cl受热易分解成NH3和HCl,二者遇冷又结合成NH4Cl,可与CaCl2分离;选项C乙醇、丁醇沸点不同可分离;D选项,溴苯中含溴单质不可用非极性溶剂萃取,若加稀NaOH溶液后,再分液可分离。
答案:D

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
 (2012?海淀区二模)最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、电解阳极发生反应,转化为乙醇和乙酸,总反应为:2CH3CHO+H2O═CH3CH2OH+CH3COOH实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示.
(2012?海淀区二模)最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、电解阳极发生反应,转化为乙醇和乙酸,总反应为:2CH3CHO+H2O═CH3CH2OH+CH3COOH实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示.