题目内容
【题目】已知反应A(g)+B(g)═C(g)+D(s) 的能量变化如图所示,下列说法正确的是( ) 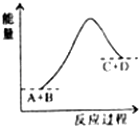
A.该反应的能量变化表现为释放能量
B.该反应中反应物A、B的总能量小于生成物C的能量
C.该反应的能量变化是将化学能转化为热能、电能等其它形式
D.该反应能量变化的实质是旧化学键断裂与新化学键形成的结果
【答案】D
【解析】解:A、图象分析可知反应过程中反应物能量低于生成物能量,反应是吸热反应,故A错误;
B、图象分析可知反应过程中反应物总能量低于生成物总能量,AB能量低于CD总能量,但该反应中反应物A、B的总能量不一定小于生成物C的能量,故B错误;
C、图象分析反应物总能量低于生成物总能量,结合能量守恒分析反应是吸热反应,该反应的能量变化是将化学能转化为热能,反应不一定是氧化还原反应,无电子转移形成电流,故C错误;
D、断裂化学键吸收能量,形成化学键放出能量,反应中断开化学键吸收的总能量高于形成化学键放出的总能量,所以形成C、D键释放的总能量大于断A、B键吸收的总能量,表现为反应吸热,该反应能量变化的实质是旧化学键断裂与新化学键形成的结果,故D正确;
故选D.
【考点精析】通过灵活运用吸热反应和放热反应,掌握化学上把吸收热量的化学反应称为吸热反应;化学上把放出热量的化学反应称为放热反应即可以解答此题.

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案【题目】表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ③ | |||||
三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
四 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:(填具体元素符号,下同).
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是 , 碱性最强的化合物的电子式是: .
(3)最高价氧化物是两性氧化物的元素是;写出它的氧化物与氢氧化钠反应的离子方程式 .
(4)用电子式表示元素④与⑥形成的化合物的形成过程 , 该化合物属于(填“共价”或“离子”)化合物.
(5)元素①的氢化物的电子式为 , 该化合物是由(填“极性”或“非极性”)键形成的.
