题目内容
在下列四种溶液中,分别加入少量固体MnO2,能产生气体的是
- A.3%H2O2溶液
- B.1 mol/L NaOH溶液
- C.1/L KClO3溶液
- D.1 mol/L盐酸
A
【错解分析】此题意在考察实验室的气体制备的常规方法及替代方法。可制备Cl2的方法有:①MnO2和浓HCl受热。②2NaCl+MnO2+2H2SO4(浓) Na2SO4+MnSO4+Cl↑+2H2O。③KMnO4、KClO3、Ca(ClO)2、K2Cr2O7等氧化浓盐酸。④电解熔解NaCl或电解饱和食盐水。
Na2SO4+MnSO4+Cl↑+2H2O。③KMnO4、KClO3、Ca(ClO)2、K2Cr2O7等氧化浓盐酸。④电解熔解NaCl或电解饱和食盐水。
【正解】A项MnO2作催化剂2H2O2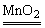 2H2O+O2↑;B项无化学反应发生;C项中2KClO3
2H2O+O2↑;B项无化学反应发生;C项中2KClO3![]() 2KCl+3O2↑,要求KClO3为固体,溶液不行;D项MnO2+4HCl(浓)
2KCl+3O2↑,要求KClO3为固体,溶液不行;D项MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,要求盐酸为浓的,且反应要加热,1mol/L的盐酸太稀,37%的盐酸物质的量浓度为12mol/L。由本题可看出:气体的制备方法要特别关注其反应物的状态、浓度及反应发生的条件。由于O2、Cl2的制备方法较多,可考点多,要给予足够的重视。可制得O2的方法除H2O2、KClO3分解之外,还可以有Na2O2与H2O或CO2反应、KMnO4受热分解、电解水等方法,F2与H2O反应可置换出O2,但不用于制备。
MnCl2+Cl2↑+2H2O,要求盐酸为浓的,且反应要加热,1mol/L的盐酸太稀,37%的盐酸物质的量浓度为12mol/L。由本题可看出:气体的制备方法要特别关注其反应物的状态、浓度及反应发生的条件。由于O2、Cl2的制备方法较多,可考点多,要给予足够的重视。可制得O2的方法除H2O2、KClO3分解之外,还可以有Na2O2与H2O或CO2反应、KMnO4受热分解、电解水等方法,F2与H2O反应可置换出O2,但不用于制备。
【错解分析】此题意在考察实验室的气体制备的常规方法及替代方法。可制备Cl2的方法有:①MnO2和浓HCl受热。②2NaCl+MnO2+2H2SO4(浓)
 Na2SO4+MnSO4+Cl↑+2H2O。③KMnO4、KClO3、Ca(ClO)2、K2Cr2O7等氧化浓盐酸。④电解熔解NaCl或电解饱和食盐水。
Na2SO4+MnSO4+Cl↑+2H2O。③KMnO4、KClO3、Ca(ClO)2、K2Cr2O7等氧化浓盐酸。④电解熔解NaCl或电解饱和食盐水。【正解】A项MnO2作催化剂2H2O2
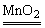 2H2O+O2↑;B项无化学反应发生;C项中2KClO3
2H2O+O2↑;B项无化学反应发生;C项中2KClO3
练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
 (选做题)
(选做题) 2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为 (用m、n表示;设A、B、C和D、E、F之间均不发生反应)。
2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为 (用m、n表示;设A、B、C和D、E、F之间均不发生反应)。