题目内容
【题目】某温度下,H2(g) + CO2(g) ![]() H2O(g)+ CO(g)的平衡常数K=9/4。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和 CO2(g),其起始浓度如下表所示
H2O(g)+ CO(g)的平衡常数K=9/4。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和 CO2(g),其起始浓度如下表所示
起始浓度 | 甲 | 乙 | 丙 |
C(H2)/ mol·l-1 | 0.010 | 0.020 | 0.020 |
C(CO2)/ mol·l-1 | 0.010 | 0.010 | 0.020 |
下列判断不正确的是
A. 平衡时,乙中CO2 的转化率大于60%
B. 平衡时,甲和丙中H2 的转化率均是60%
C. 平衡时,丙中C(CO2)是甲中的2倍,是0.012 mol·l-1
D. 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
【答案】C
【解析】某温度下,H2(g) + CO2(g) ![]() H2O(g)+ CO(g)的平衡常数K=9/4。该反应是一个气体分子数不变的反应,所以压强不影响该反应的化学平衡状态。由甲的投料和该反应的平衡常数可以计算出,氢气和二氧化碳的平衡浓度都是0.004mol/L(设二氧化碳的变化量为x,则
H2O(g)+ CO(g)的平衡常数K=9/4。该反应是一个气体分子数不变的反应,所以压强不影响该反应的化学平衡状态。由甲的投料和该反应的平衡常数可以计算出,氢气和二氧化碳的平衡浓度都是0.004mol/L(设二氧化碳的变化量为x,则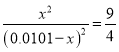 ,解之得x=0.006mol/L),氢气和二氧化碳的转化率均为
,解之得x=0.006mol/L),氢气和二氧化碳的转化率均为![]() 60%,丙和甲的投料的比例是相同的,所以丙和甲能建立等效平衡,丙和甲的反应物的转化率是相同的,但是它们的平衡浓度不同,丙中C(CO2)是甲中的2倍,是0.008 mol·l-1 。A. 平衡时,乙相当于在甲的平衡状态下再增大反应物氢气的浓度,化学平衡向正反应方向移动,所以乙中CO2 的转化率大于60%,A正确;B. 平衡时,甲和丙中H2 的转化率均是60%,B正确;C. 平衡时,丙中C(CO2)是甲中的2倍,是0.008 mol·l-1 ,C不正确;D. 反应开始时,丙中的反应物浓度最大,反应速率最快;甲中的反应物浓度最小,反应速率最慢,D正确。本题选C。
60%,丙和甲的投料的比例是相同的,所以丙和甲能建立等效平衡,丙和甲的反应物的转化率是相同的,但是它们的平衡浓度不同,丙中C(CO2)是甲中的2倍,是0.008 mol·l-1 。A. 平衡时,乙相当于在甲的平衡状态下再增大反应物氢气的浓度,化学平衡向正反应方向移动,所以乙中CO2 的转化率大于60%,A正确;B. 平衡时,甲和丙中H2 的转化率均是60%,B正确;C. 平衡时,丙中C(CO2)是甲中的2倍,是0.008 mol·l-1 ,C不正确;D. 反应开始时,丙中的反应物浓度最大,反应速率最快;甲中的反应物浓度最小,反应速率最慢,D正确。本题选C。

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】工业上通常采用CO(g)和H2(g)催化合成甲醇CH3OH(g).
(1)在—定温度和压强下,CO(g)+2H2(g)![]() CH3OH(g) ΔH=-128.8 kJ/mol.若将10a mol CO和20a mol H2放入2 L的密闭容器中,充分反应后测得CO的转化率为60%,则该反应的平衡常数为________(用含a的代数式表示).若此时再向该容器中投入10a mol CO、20a mol H2和10a mol CH3OH(g),判断平衡移动的方向是_______(填“正向移动”、“逆向移动”或“不移动”)。
CH3OH(g) ΔH=-128.8 kJ/mol.若将10a mol CO和20a mol H2放入2 L的密闭容器中,充分反应后测得CO的转化率为60%,则该反应的平衡常数为________(用含a的代数式表示).若此时再向该容器中投入10a mol CO、20a mol H2和10a mol CH3OH(g),判断平衡移动的方向是_______(填“正向移动”、“逆向移动”或“不移动”)。
(2)判断该反应达到平衡状态的依据是________(填字母序号).
A.混合气体的密度不变
B.混合气体的平均相对分子质量不变
C.2v逆(H2)=v正(CO)
D.容器内CO、H2、CH3OH的浓度之比为1∶2∶1
E.CH3OH、CO、H2的浓度都不再发生变化
(3)一定条件下,在容积相同的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器 | 甲 | 乙 | 丙 | |
反应物投入量 | 1 mol CO、2 mol H2 | 1 mol CH3OH | 2 mol CH3OH | |
平衡时数据 | 反应能量变化的绝对值(kJ) | a | b | c |
反应物转化率 | α1 | α2 | α3 | |
体系压强(Pa) | p1 | p2 | p3 | |
则a+b=________;a1+a3________1(填“<”、“>”或“=”,下同);2p2________p3.
【题目】现使用酸碱中和滴定法测定市售白醋的总酸量(g·100 mL-1)。
Ⅰ.实验步骤:
(1)配制待测白醋溶液。用________________(填仪器名称)量取10.00 mL食用白醋,在__________(填仪器名称)中用水稀释后转移到100 mL__________(填仪器名称)中定容,摇匀即得待测白醋溶液。
(2)量取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴酚酞作指示剂。
(3)读取盛装0.100 0 mol·L-1NaOH 溶液的碱式滴定管的初始读数。
(4)滴定。判断滴定终点的现象是:_________________,到达滴定终点,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
(5)如图是某次滴定时的滴定管中的液面,其读数为________mL。
![]()
Ⅱ.实验记录
实验数据(mL) 滴定次数 | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论:
(1)甲同学在处理数据时计算得:平均消耗的NaOH溶液的体积V= mL=15.24 mL。指出他计算的不合理之处:______。按正确数据处理,得c(市售白醋)=_____mol·L-1;市售白醋总酸量=_____g·100 mL-1。
mL=15.24 mL。指出他计算的不合理之处:______。按正确数据处理,得c(市售白醋)=_____mol·L-1;市售白醋总酸量=_____g·100 mL-1。
(2)乙同学仔细研究了该品牌白醋的标签,发现其中还含有苯甲酸钠作为食品添加剂,他想用资料法验证醋酸与苯甲酸钠不会发生复分解反应,需查找在一定温度下的________(填序号)。
A.pH B.电离度 C.电离平衡常数 D.溶解度
(3)在本实验的滴定过程中,下列操作会使实验结果偏大的是_________(填写序号)。
A.碱式滴定管在滴定时未用标准NaOH溶液润洗
B.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
C.锥形瓶中加入待测白醋溶液后,再加少量水
D.锥形瓶在滴定时剧烈摇动,有少量液体溅出
【题目】已知水在25℃和T℃时,其电离平衡曲线如图所示:

(1)25℃时,有pH=12的Ba(OH)2溶液。
①该Ba(OH)2溶液的物质的量浓度为__________________;
②25℃时,向100mLpH=2的硫酸与硫酸钠的混合溶液中,加入300mL上述Ba(OH)2溶液,沉淀正好达最大量( 假设溶液混合前后的体积变化忽略不计),原混合溶液中硫酸钠的物质的量浓度为_______________。
(2)T℃时,将100 mL pH=5的硫酸溶液稀释至原体积的1000倍,稀释后溶液中c(H+)/c(SO42-)=____________。
(3)T℃时,将0.1 mol·L-1的NaHSO4溶液与0.1 mol·L-1的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
甲 | 乙 | 丙 | 丁 | |
0.1 mol·L-1 Ba(OH)2溶液体积/mL | 10 | 10 | 10 | 10 |
0.1 mol·L-1 NaHSO4溶液体积/mL | 5 | 10 | 15 | 20 |
①按丁方式混合后,所得溶液显________________(填“酸”、“碱”或“中”)性。
②写出按乙方式混合后,反应的离子方程式:_________________________。
③按甲方式混合后,所得溶液的pH为______________________。
