题目内容
【题目】X、Y、Z和W代表原子序数依次增大的四种短周期主族元素.它们满足以下条件:①在元素周期表中,Z与Y、W均相邻;②X、Y、W分别位于不同周期;③Y、Z、W三种元素的原子最外层电子数之和为17。下列说法错误的是
A. X、Y、Z既能形成离子化合物,又能形成共价化合物
B. Y和Z元素的原子半径大小顺序为Y>Z
C. X与Y、Z之间形成的核外电子总数为10的微粒只有YX3和X2Z
D. Z、W元素的最简单氢化物的沸点和稳定性均为H2Z>H2W
【答案】C
【解析】
X、Y、Z和W代表原子序数依次增大的四种短周期主族元素,在元素周期表中,Z与Y、W均相邻,Y、Z、W三种元素的原子最外层电子数之和为17,若Y、Z、W三者处于同一周期或同一主族,最外层电子数之和不可能为17,处于不同周期的Y、Z、W两两相邻,可能出现的位置关系有: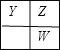 、
、![]() ,设Y的最外层电子数为x,若为第一种情况,则有x+x+1+x+1=17,解得x=5,Y、Z、W对应的三种元素分别为N,O,S;若为第二种情况,则有x+x+x+1=17,解得x=
,设Y的最外层电子数为x,若为第一种情况,则有x+x+1+x+1=17,解得x=5,Y、Z、W对应的三种元素分别为N,O,S;若为第二种情况,则有x+x+x+1=17,解得x=![]() ,不合理,且X、Y、W分别位于不同周期,则X为H元素,据此解答。
,不合理,且X、Y、W分别位于不同周期,则X为H元素,据此解答。
A. X、Y、Z可形成的化合物可为HNO3或NH4NO3等,前者为共价化合物,后者为离子化合物,A项正确;
B. Y、Z位于同一周期,同周期元素从左到右原子半径逐渐减小,则原子半径大小顺序为:Y>Z,B项正确;
C. H与N、O元素之间形成的核外电子总数为10的微粒有NH3、NH4+、OH、H2O、H3O+等,C项错误;
D. Z、W分别为O、S元素,其氢化物分别为水、硫化氢,非金属性越强,氢化物稳定性越强,水分子之间存在氢键,则二者最简单氢化物的沸点和稳定性均为H2Z>H2W,D项正确;
答案选C。

 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
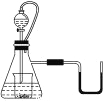
芒果教辅暑假天地重庆出版社系列答案【题目】向如图所示装置中缓慢通入气体X,若打开活塞K,则品红溶液褪色;若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊。X和Y可能是
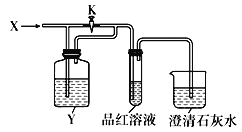
选项 | A | B | C | D |
X | SO2 | Cl2 | HCl | Cl2 |
Y | NaOH溶液 | 饱和NaHCO3溶液 | 饱和NaCl溶液 | Na2SO3溶液 |
A. A B. B C. C D. D
【题目】下表为元素周期表的一部分,表中列出12种元素在周期表中的位置,按要求回答下列各题:
周期族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ⑦ | ⑨ | ||||||
3 | ② | ④ | ⑥ | ⑧ | ⑩ | |||
4 | ③ | ⑤ |
(1)这12种元素中,化学性质最不活泼的元素是______(填元素符号或化学式,下同),得电子能力最强的原子是______,失电子能力最强的单质与水反应的离子反应方程式是____,常温下单质为液态的非金属单质是____________。
(2)元素⑤的离子结构示意图为__________________。
(3)写出⑦⑧⑨与①形成的简单化合物中最稳定的分子式________。写出⑧⑩两种元素最高价氧化物对应水化物中酸性较弱的化学式________。
(4)写出⑨⑩与①形成的化合物中沸点最低的化学式______酸性最强的化学式_______。
(5)写出④的单质置换出⑦的单质的化学反应方程式:__________________。
②和⑥两种元素最高价氧化物对应的水化物相互反应的离子方程式为__________。
③和⑩两种元素最高价氧化物对应的水化物相互反应的离子方程式为__________。
用电子式表示⑤与⑨组成的二元化合物的形成过程_____________________。