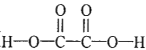题目内容
【题目】A+、B2+、C-、D2-4种离子具有相同的电子层结构。现有以下排列顺序:
①B2+>A+>C->D2-②C->D2->A+>B2+③B2+>A+>D2->C-④D2->C->A+>B2+4种离子的半径由大到小以及4种元素原子序数由大到小的顺序分别是( )
A.①④B.④①C.②③D.③②
【答案】B
【解析】
A+、B2+、C-、D2-四种离子具有相同的电子层结构,核外电子数相等,令核外电子数为x,则A、B、C、D的原子序数分别为x+1、x+2、x-1、x-2,故原子序数(核电荷数)B2+>A+>C->D2-;电子层结构相同,核电荷数越大离子半径越小,故离子半径D2->C->A+>B2+,故选B。

【题目】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O)晶体,设计了如下流程:

已知:(1)常温下,金属离子开始沉淀和沉淀完全时的pH 见下表。
开始形成氢氧化物沉淀的pH | 完全形成氢氧化物沉淀的pH | |
Fe2+ | 7.0 | 9.0 |
Fe3+ | 1.9 | 3.2 |
Al3+ | 3.3 | 5.0 |
(2)七水合硫酸亚铁(FeSO4·7H2O)的溶解度
温度/℃ | 10 | 20 | 30 | 40 | 50 |
FeSO4·7H2O溶解度(g) | 15.5 | 26.5 | 32.9 | 40.2 | 48.9 |
(1)溶解烧渣选用足量硫酸,写出Fe2O3与硫酸反应的离子方程式_______________;检验溶液1中含有Fe3+的实验方法是___________________;
(2)固体1是制作单晶硅的主要原料,写出该反应的化学方程式___________________;
(3)试剂X是__________________;固体2是___________________;
(4)加入NaOH溶液控制pH应不超过_________________;
(5)从溶液2中获得晶体的的方法为______________, _____________过滤、洗涤、干燥。
【题目】在1.0L密闭容器中放入0.10 molA(g),在一定温度进行如下反应:A(g) ![]() B(g)+C(g)△H=+85.1kJmol-1,反应时间(t)与容器内气体总压强(p)的数据见下表:
B(g)+C(g)△H=+85.1kJmol-1,反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
总压强p/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为 ______ 。
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为 ______,平衡时A的转化率为 ______。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总= ______ mol,n(A)= ______ mol。
②下表为反应物A浓度与反应时间的数据,计算:α= ______。
反应时间t/h | 0 | 4 | 8 | 16 |
c(A)/(molL-1)) | 0.10 | a | 0.026 | 0.0065 |
分析该反应中反应物的浓度c(A)变化与时间间隔(△t)的规律,得出的结论是 ______,由此规律推出反应在12h时反应物的浓度c(A)为 ______ mol·L-1。