题目内容
【题目】下图中 A、B、C、D 分别是三种烃的分子结构,请回答下列问题:
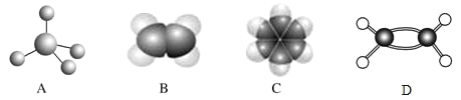
(1)上图中 D 是有机物分子的_____模型;
(2)烃 A 及其同系物的分子式符合通式_____(碳原子个数用 n 表示),当 n=6 时的同分异构体数目为_____(填数字)种;
(3)上述三种有机物烃中,所有原子均共平面的是_________(填有机物的名称);
(4)下列关于烃 C 的叙述正确的是_____(填序号)。
A.分子式为 C6H6,它不能使酸性 KMnO4 溶液褪色,属于饱和烃
B.从分子结构看,C 分子中含有碳碳双键,属于烯烃
C.烃 C 的同系物二甲苯(C8H10)有三种不同的结构,均属于芳香烃
D.烃 C 中加入溴水,充分振荡,静置,下层无色
(5)分别写出 B 使溴水褪色、C 的溴代反应的化学方程式____________、_____________,并指明反应类型:________________、______________
(6)C 的同系物甲苯与足量氢气加成后的产物(甲基环己烷)的一氯代物有_____种。
【答案】球棍 CnH2n+2(n≥1) 5 乙烯、苯 CD CH2=CH2+Br2→CH2Br—CH2Br ![]() +Br2
+Br2![]()
![]() +HBr 加成反应 取代反应 5
+HBr 加成反应 取代反应 5
【解析】
根据图示,A为甲烷分子的球棍模型,B为乙烯分子的比例模型,C为苯分子的球棍模型,D为乙烯分子的球棍模型,根据以上有机物的结构与性质分析解答下列问题。
(1)根据分析D为乙烯分子的球棍模型;
(2) A为甲烷,及其同系物属于烷烃,烷烃的分子式通式CnH2n+2(n≥1);当 n=6 时,该烃的分子式为C6H14的烷烃,己烷的同分异构体分别为:主链为6个碳原子时CH3CH2CH2CH2CH2CH3;主链为5个碳原子时:(CH3)2CHCH2CH2CH3、CH3CH2CH(CH3)CH2CH3;主链为4个碳原子时:(CH3)2CHCH(CH3)2、(CH3)3CCH2CH3,共有5种;
(3)上述三种有机物烃中,A为甲烷是正四面体结构,所有原子不在同一平面,B为乙烯,是平面结构,所有原子在同一平面,C为苯,是平面结构,所有原子在同一平面,则所有原子均共平面的是乙烯、苯;
(4) C为苯,苯分子结构中,不含碳碳单键和双键,是一种介于单键与双键之间的一种特殊键,在一定条件下能发生加成反应、取代反应、氧化反应,但不能使酸性高锰酸钾溶液褪色;
A.苯分子式为 C6H6,它不能使酸性 KMnO4 溶液褪色,能发生加成反应,则属于不饱和烃,故A错误;
B.苯分子结构中,不含碳碳单键和双键,是一种介于单键与双键之间的一种特殊键,属于芳香烃,故B错误;
C.苯分子的结构为平面的正六边形,两个甲基在苯环上有邻间对三个位置结构,分别为邻二甲苯、间二甲苯、对二甲苯,含有苯环的烃类均属于芳香烃,故C正确;
D.苯与溴水不反应,由于溴水中的溴单质在苯中的溶解度较大,故向溴水中加入苯,充分混合振荡静置后,溴单质会转移至溶解度较大的苯中,由于苯的密度比水小,且不溶于水, 溶液分层,上层是苯层,由于溶解溴单质为橙色,下层为水层,几乎无色,故D正确;
答案选CD;
(5)乙烯结构中含有碳碳双键,和溴水发生加成反应,使溴水褪色,方程式为CH2=CH2+Br2→CH2Br—CH2Br;苯和溴单质在溴化铁作催化剂的作用下发生取代反应,生成溴苯和溴化氢,化学方程式为![]() +Br2
+Br2![]()
![]() +HBr;
+HBr;
(6)苯的同系物甲苯与足量氢气加成后的产物(甲基环己烷)由一个甲基和六元环构成,甲基环己烷中有5种不同环境的氢原子,如图所示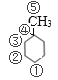 ,则其一氯代物由5种。
,则其一氯代物由5种。

 阅读快车系列答案
阅读快车系列答案