题目内容
下列物质中,在一定条件下能发生取代反应和加成反应,但不能使酸性高锰酸钾溶液褪色的是
| A.乙烷 | B.甲烷 | C.苯 | D.乙烯 |
C
解析试题分析:A、乙烷能和氯气在光照的条件下发生取代反应,它属于饱和烃,不能发生加成反应,不能被高锰酸钾氧化,故A错误;B、甲烷能和氯气在光照的条件下发生取代反应,它属于饱和烃,不能发生加成反应,不能被高锰酸钾氧化,故B错误;C、苯的化学性质特点是:易取代难加成,可以和溴发生取代反应生成溴苯,可以和氢气发生加成反应生成环己烷,不能使酸性高锰酸钾溶液褪色,故C正确;D、乙烯能被高锰酸钾氧化为二氧化碳,能使高锰酸钾褪色,故D错误,故选C。
考点:考查有机物的化学性质和有机反应类型

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案乙烯是来自石油的重要有机化工原料,其产量通常用来衡量一个国家的石油化工发展水平。结合以下路线回答:
已知: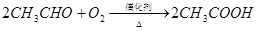
(1)反应II的化学方程式是 。
(2)D为高分子化合物,可以用来制造多种包装材料,其结构简式是 。
(3)E是有香味的物质,在实验室用下图装置制取。
①反应IV的化学方程式是 ,该反应类型为 。
②该装置图中有一个明显的错误是 。
(4)为了证明浓硫酸在反应IV中起到了催化剂和吸水剂的作用,某同学利用上图改进后装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管乙再测有机层的厚度,实验记录如下:
| 实验编号 | 试管甲中试剂 | 试管乙中试剂 | 有机层的厚度/cm |
| A | 2 mL乙醇、1 mL乙酸、 1mL18mol·L-1浓硫酸 | 饱和Na2CO3溶液 | 3.0 |
| B | 2 mL乙醇、1 mL乙酸 | 0.1 | |
| C | 2 mL乙醇、1 mL乙酸、 3 mL 2mol·L-1 H2SO4 | 0.6 | |
| D | 2 mL乙醇、1 mL乙酸、盐酸 | 0.6 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是3mL和 mol·L-1。
②分析实验 (填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
含有一个双键的烯烃,和氢加成后的产物结构简式如图,则此烃可能有的结构有( )
| A.4种 | B.5种 | C.6种 | D.7种 |
下列过程前者属于物理变化,后者属于化学变化的是
| A.碳酸钠晶体的风化、硫酸铜检验水 |
| B.煤的干馏、石油的裂化 |
| C.碘的升华、熔融的氯化镁导电 |
| D.煤的气化、用浸泡过高锰酸钾溶液的硅藻土保鲜水果 |
区别CH4和C2H4的方法最好是
| A.比较它们在水中的溶解度大小 | B.嗅闻它们的气味 |
| C.通入溴水中观察溶液颜色的变化 | D.点燃它们后,观察火焰 |
下列物质在一定条件下,可与苯发生化学反应的是 ( )
| A.水 | B.溴水 | C.浓硝酸 | D.酸性高锰酸钾溶液 |
下列文字表述与反应方程式对应不正确的是( )
| A.氯气和水反应:Cl2+ H2O = 2H+ + Cl-+ ClO- |
| B.用醋酸除去水垢:CaCO3 + 2CH3COOH = Ca2+ +2CH3COO-- + H2O + CO2↑ |
| C.将丙烯通入溴水中:CH3—CH=CH2 +Br2→ CH3CHBrCH2Br |
D.甲烷与氧气反应:CH4+ 2O2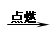 CO2 + 2H2O CO2 + 2H2O |
 ,它可通过不同化学反应分别制得B、C和D三种物质.
,它可通过不同化学反应分别制得B、C和D三种物质.

