题目内容
【题目】(1)写出CO2和Na2O2反应的化学方程式:_______________。
(2)某学生判断SO2和Na2O2反应能生成硫酸钠,你认为他的判断合理吗?________,简要说明理由:__________________________。
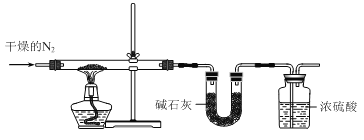
(3)该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(图中铁架台等装置已略去)。

装置中B的作用是__________________,D的作用是_______________。
(4)为确认反应产物,该同学设计了以下实验步骤,你认为应进行的操作按顺序排列是(选填序号)________。
A.用带火星的细木条靠近干燥管口a,观察细木条是否着火燃烧
B.将C装置中反应后的固体物质溶于适量水配成溶液
C.在配成的溶液中加入用硝酸酸化的硝酸钡溶液,观察是否有沉淀生成
D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成
【答案】(1)2CO2+2Na2O2===2Na2CO3+O2;(2)合理,由于过氧化钠具有强氧化性,能将+4价的硫氧化为+6价的硫而生成硫酸钠;(3)干燥SO2气体,防止水蒸气进入C装置与Na2O2反应 防止空气中的水蒸气和CO2进入C装置与Na2O2反应生成氧气,同时吸收过量SO2气体,便于氧气的检验和防止污染空气;(4)ABD。
【解析】
试题分析:(1)Na2O2和CO2发生反应:2Na2O2+2CO2=2Na2CO3+O2;(2)过氧化钠能和水、CO2反应,同时过氧化钠具有强氧化性,SO2以还原性为主,两者发生反应Na2O2+SO2=Na2SO4;(3)装置B中盛放浓硫酸,作用是干燥SO2,因为Na2O2能和水、CO2反应,因此避免对实验的干扰,装置D的作用是防止空气的水蒸气和CO2进入装置C,同时吸收SO2气体,防止污染空气;(4)A、如果带火星的木条复燃,说明有氧气产生,发生2Na2O2+2SO2=2Na2SO3+O2,故正确;B、溶于水后产生气体,说明含有过氧化钠,故正确;C、硝酸具有强氧化性,能把Na2SO3氧化成Na2SO4,产生干扰,故错误;D、加入盐酸,除去干扰离子,再加入BaCl2溶液,出现沉淀,说明含有Na2SO4,故正确。

 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案