ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩœ¬±μ «‘ΣΥΊ÷ήΤΎ±μΒΡ“Μ≤ΩΖ÷Θ§’κΕ‘±μ÷–ΒΡΔΌΓΪΔα÷÷‘ΣΥΊΘ§Χν–¥œ¬Ν–Ω’ΑΉΘΚ
÷ςΉε | ΔώA | ΔρA | ΔσA | ΔτA | ΔθA | ΔωA | ΔςA | 0Ήε |
2 | ΔΌ | ΔΎ | Δέ | |||||
3 | Δή | Δί | Δό | ΔΏ | Δύ | |||
4 | Δα |
Θ®1Θ©’β–©‘ΣΥΊ÷–Θ§Μ·―ß–‘÷ Ήν≤ΜΜνΤΟΒΡ «Θ®Χν‘ΣΥΊΖϊΚ≈Θ§œ¬Ά§Θ©Θ°
Θ®2Θ©ΉνΗΏΦέ―θΜ·ΈοΒΡΥ°Μ·Έο÷–Θ§Υα–‘Ήν«ΩΒΡΜ·ΚœΈοΒΡΜ·―ß ΫΘΚ Θ§ Φν–‘Ήν«ΩΒΡΜ·ΚœΈοΒΡΒγΉ” ΫΘΚ Θ°
Θ®3Θ©ΉνΗΏΦέ―θΜ·Έο «ΝΫ–‘―θΜ·ΈοΒΡ‘ΣΥΊ « Θ°
Θ®4Θ©”ΟΒγΉ” Ϋ±μ Ψ‘ΣΥΊΔή”κΔό–Έ≥…Μ·ΚœΈοΒΡΙΐ≥ΧΘΚ Θ°
Θ®5Θ©ΔΌ”κΔΏ–Έ≥…ΒΡΜ·ΚœΈοΒΡΒγΉ” ΫΘΚ Θ§ ΗΟΜ·ΚœΈο «”…Θ®ΧνΓΑΦΪ–‘Γ±ΜρΓΑΖ«ΦΪ–‘Γ±Θ©Ι≤ΦέΦϋ–Έ≥…ΒΡΘ°
ΓΨ¥πΑΗΓΩ
Θ®1Θ©Ar
Θ®2Θ©HClO4ΘΜ![]()
Θ®3Θ©Al
Θ®4Θ©![]()
Θ®5Θ©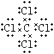 ΘΜΦΪ–‘
ΘΜΦΪ–‘
ΓΨΫβΈωΓΩΫβΘΚ”…‘ΣΥΊ‘Ύ÷ήΤΎ±μ÷–ΒΡœύΕ‘ΈΜ÷ΟΩ…÷ΣΘΚΔΌ «CΘ§ΔΎ «NΘ§Δέ «OΘ§Δή «NaΘ§Δί «AlΘ§Δό «SΘ§ΔΏ «ClΘ§Δύ «ArΘ§Δα «KΘ§Θ®1Θ©’β–©‘ΣΥΊ÷–Θ§Μ·―ß–‘÷ Ήν≤ΜΜνΤΟΒΡ «ArΘ§Υυ“‘¥πΑΗ «ΘΚArΘΜΘ®2Θ©…œ ω‘ΣΥΊ÷–ΗΏ¬»ΥαΈΣΚ§―θΥα÷–Υα–‘Ήν«ΩΒΡΥαΘ§ΤδΜ·―ß ΫΈΣHClO4 Θ§ KOHΒΡΦν–‘Ήν«ΩΘ§ΤδΒγΉ” ΫΈΣ ![]() Θ§Υυ“‘¥πΑΗ «ΘΚHClO4ΘΜ
Θ§Υυ“‘¥πΑΗ «ΘΚHClO4ΘΜ ![]() ΘΜΘ®3Θ©―θΜ·Έο÷–―θΜ·¬ΝΈΣΝΫ–‘―θΜ·ΈοΘ§‘ρΉνΗΏΦέ―θΜ·Έο «ΝΫ–‘―θΜ·ΈοΒΡ‘ΣΥΊ «AlΘ§Υυ“‘¥πΑΗ «ΘΚAlΘΜΘ®4Θ©Δή”κΔό–Έ≥…Μ·ΚœΈοΈΣNa2SΘ§ΒγΉ” Ϋ±μ ΨΜ·ΚœΈοΒΡ–Έ≥…Ιΐ≥ΧΈΣ
ΘΜΘ®3Θ©―θΜ·Έο÷–―θΜ·¬ΝΈΣΝΫ–‘―θΜ·ΈοΘ§‘ρΉνΗΏΦέ―θΜ·Έο «ΝΫ–‘―θΜ·ΈοΒΡ‘ΣΥΊ «AlΘ§Υυ“‘¥πΑΗ «ΘΚAlΘΜΘ®4Θ©Δή”κΔό–Έ≥…Μ·ΚœΈοΈΣNa2SΘ§ΒγΉ” Ϋ±μ ΨΜ·ΚœΈοΒΡ–Έ≥…Ιΐ≥ΧΈΣ ![]() Υυ“‘¥πΑΗ «ΘΚ
Υυ“‘¥πΑΗ «ΘΚ ![]() ΘΜΘ®5Θ©ΔΌ”κΔΏ–Έ≥…ΒΡΜ·ΚœΈοΈΣCCl4 Θ§ ΈΣΙ≤ΦέΜ·ΚœΈοΘ§Ης‘≠Ή”¬ζΉψ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§ΒγΉ” ΫΈΣ
ΘΜΘ®5Θ©ΔΌ”κΔΏ–Έ≥…ΒΡΜ·ΚœΈοΈΣCCl4 Θ§ ΈΣΙ≤ΦέΜ·ΚœΈοΘ§Ης‘≠Ή”¬ζΉψ8ΒγΉ”Έ»Ε®ΫαΙΙΘ§ΒγΉ” ΫΈΣ 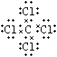 Θ§÷ΜΜΜC©¹ClΦΪ–‘Ι≤ΦέΦϋΘ§Υυ“‘¥πΑΗ «ΘΚ
Θ§÷ΜΜΜC©¹ClΦΪ–‘Ι≤ΦέΦϋΘ§Υυ“‘¥πΑΗ «ΘΚ 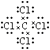 ΘΜΦΪ–‘Θ°
ΘΜΦΪ–‘Θ°


