题目内容
【题目】已知某微粒的结构示意图为: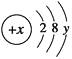 (y ≠ 0 )。请回答:
(y ≠ 0 )。请回答:
(1)当x-y=10时,该微粒为________(填“原子”、“阳离子”或“阴离子”)。
(2)当y=8时,微粒可能为(不少于5种)___________________。
(3)写出x+y=12与x+y=16的元素最高价氧化物对应水化物相互反应的离子方程式 _。
【答案】(1)原子(2)氩原子、氯离子、硫离子、钾离子、钙离子等
(3)Al(OH)3+OH-=AlO2-+2H2O
【解析】试题分析:(1)当x-y=10时,该微粒的核内质子数等于核外电子数,为原子;(2)当y=8时,为18电子的粒子,可能为氩原子、氯离子、硫离子、钾离子、钙离子等;(3)x+y=12,则x=11,y=1,为钠;x+y=16,则x=13,y=3,为Al;最高价氧化物对应水化物相互
反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】某同学做同周期元素性质递交规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:
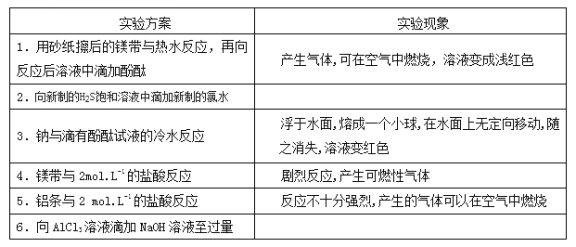
请你帮助该同学整理并完成实验报告
(1)实验目的:验证同周期元素金属性、非金属性的变化规律。
(2)实验用品:略。
(3)实验内容:(填写题给信息表中相应的实验现象,并在有空格处写出相对应的离子方程式)
实验方案 | 实验现象 | 有关离子方程式 |
不填 | 不填 | |
② | ______________ | ______________ |
不填 | ______________ | |
④ | 不填 | 不填 |
⑤ | 不填 | ______________ |
⑥ | ______________ | ______________ |
(4)实验结论:______________。
(5)问题与讨论:
请从原子结构理论上简单说明具有上述结论的原因是___________________。