题目内容
【题目】将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) ![]() 2C(g)。若经2s后测得C的浓度为0.6mol/L,现有几种说法:
2C(g)。若经2s后测得C的浓度为0.6mol/L,现有几种说法:
①用物质A表示的反应的平均速率为0.3 mol/(Ls)
②用物质B表示的反应的平均速率为0.6 mol/(Ls)
③2s时物质A的转化率为70%
④2s时B物质的浓度为0.7 mol/L 其中正确的是( )
A. ①③B. ①④C. ②③D. ③④
【答案】B
【解析】
根据化学反应速率等于单位时间内浓度的变化量及根据反应2A(g)+B(g)2C(g),并利用三段式法计算,据此解答。
利用三段式法计算:
起始A的浓度为![]() = 2mol/L,B的浓度为
= 2mol/L,B的浓度为![]() = 1mol/L,则列出三段式如下:
= 1mol/L,则列出三段式如下:
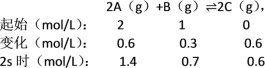
2s内,用物质A表示的反应的平均速率为v(A)=![]() = 0.3molL-1s-1;
= 0.3molL-1s-1;
2s内,用物质B表示的反应的平均速率为v(B)=![]() = 0.15molL-1s-1;
= 0.15molL-1s-1;
2s时物质A的转化率为α=![]() ×100% = 30%;
×100% = 30%;
2s时物质B的浓度为0.7 molL-1,
显然①④正确,
答案选B。

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
【题目】下表为元素周期表的一部分,回答下列有关问题(填写化学符号):
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ⑴ | ⑻ | ⑵ | |||||
三 | ⑶ | ⑷ | ⑸ | ⑹ | ⑺ | ⑼ | ||
四 | ⑽ | ⑾ | ⑿ |
(1)⑴-⑿元素的最高价氧化物对应的水化物中,酸性最强的是______,碱性最强的是_____。
(2)元素⑼在周期表中的位置_______________,若⑻的一种核素中含有10个中子,用![]() 表示该原子:______________。
表示该原子:______________。
(3)在⑴-⑿元素中,原子半径最小的是______________,原子半径最大的是__________。
(4)第三周期简单阴离子半径最大的离子是____________