题目内容
【题目】运用化学反应原理研究碳、氮的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。
(1) 用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的 活性炭和NO,发生 反应C(s)+2NO(g) ![]() N2(g)+CO2(g)△H=QkJ/mol。 在T1℃时,反应进行到不同时间(min) 测得各物质的浓度(mol/L) 如下:
N2(g)+CO2(g)△H=QkJ/mol。 在T1℃时,反应进行到不同时间(min) 测得各物质的浓度(mol/L) 如下:
浓度 时间 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①30min 后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是________(填字母编号)
a.通入一定量的NO b.加入定量的活性炭
c.加入合适的催化剂 d.适当缩小容器的体积
② 若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3: 1: 1,则Q_____ 0 (填“>”或“<”<)。
(2) 某研究小组在实验室用某新型催化剂对CO、NO催化转化进行研究,则得NO转化为N2的转化率随温度、CO混存量的变化情况如下图所示,利用以下反应:NO+CO![]() N2+CO2( 有CO) 2NO
N2+CO2( 有CO) 2NO![]() N2+ O2 (无CO)
N2+ O2 (无CO)

①若不使用CO,温度超过775℃,发现NO的分解率降低,其可能的原因为: __________;在n(NO)/n(CO)= 1的条件下,应控制最佳温度在_______左右。
②用CxHy(烃)催化还原NOx也可消除氮氧化物的污染,写出C2H6与NO2发生反应的化学方程式_________________。
③以NO2、O2 熔融NaNO3
(3) 天然气的一个重要用途是制取氢气,其原理如下:

已知:① 2CO(g)+O2(g)=2CO2(g) △H1
②CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) △H2
③2H2(g)+O2(g)=2H2O(l) △H3
1)科学家提出一种利用天然气制备氢气的方法: CH4(g)+ CO2(g)=2CO(g)+2H2(g) △H=_____
2)这种方法的推广与使用,不仅实现资源综合利用,而且还能解决环境问题是_________。
【答案】 ad < 该反应是放热反应,升高温度反应更有利于向逆反应方向进行 870℃ (850℃到900℃之间都可以) 4C2H6+ 14NO2![]() 8CO2+7N2+12H2O NO2+ NO3--e-=N2O5 △H=△H2-△H1-△H3 减少温室气体排放,缓解温室效应
8CO2+7N2+12H2O NO2+ NO3--e-=N2O5 △H=△H2-△H1-△H3 减少温室气体排放,缓解温室效应
【解析】试题分析:本题考查图像和图表的分析,外界条件对化学平衡的影响,化学方程式的书写,盖斯定律的应用,原电池原理和电极反应式的书写。
(1)①根据表格20min和30min时各物质的浓度分别对应相等,20min时已经达到平衡;40min和50min时各物质的浓度分别对应相等,40min时又再次达到平衡;30min时改变条件,达到新平衡时NO浓度增大为原来的0.60![]() 0.50=1.2倍,N2和CO2的浓度增大为原来的0.3
0.50=1.2倍,N2和CO2的浓度增大为原来的0.3![]() 0.25=1.2倍。a项,通入一定量NO,平衡正向移动,达到新平衡时NO、N2、CO2的浓度都可能为原来的1.2倍(由于C为固体,相当于增大压强平衡不移动);b项,加入定量活性炭,平衡不移动,各物质物质的量浓度不变;c项,加入合适催化剂,加快反应速率,平衡不移动,各物质物质的量浓度不变;d项,适当缩小容器体积,平衡不移动,由于体积减小,达到新平衡时NO、N2、CO2的浓度都可能为原来的1.2倍;30min改变的条件可能是通入一定量的NO、适当缩小容器的体积,答案选ad。
0.25=1.2倍。a项,通入一定量NO,平衡正向移动,达到新平衡时NO、N2、CO2的浓度都可能为原来的1.2倍(由于C为固体,相当于增大压强平衡不移动);b项,加入定量活性炭,平衡不移动,各物质物质的量浓度不变;c项,加入合适催化剂,加快反应速率,平衡不移动,各物质物质的量浓度不变;d项,适当缩小容器体积,平衡不移动,由于体积减小,达到新平衡时NO、N2、CO2的浓度都可能为原来的1.2倍;30min改变的条件可能是通入一定量的NO、适当缩小容器的体积,答案选ad。
②30min时容器中NO、N2、CO2的浓度之比为0.50:0.25:0.25=2:1:1,升高温度达到平衡时容器中NO、N2、CO2的浓度之比为3:1:1,升高温度平衡向逆反应方向移动,逆反应为吸热反应,正反应为放热反应,Q![]() 0。
0。
(2)①若不使用催化剂,发生的反应为2NO![]() N2+O2,温度超过775℃,NO的分解率降低,可能原因是:该反应是放热反应,升高温度更有利于反应向逆反应方向进行。根据图像当n(NO)/n(CO)=1时,870℃左右NO的转化率最大,所以应控制的最佳温度在870℃左右。
N2+O2,温度超过775℃,NO的分解率降低,可能原因是:该反应是放热反应,升高温度更有利于反应向逆反应方向进行。根据图像当n(NO)/n(CO)=1时,870℃左右NO的转化率最大,所以应控制的最佳温度在870℃左右。
②烃催化还原NOx可消除氮氧化物的污染,氮氧化物被还原为N2,则烃转化成CO2和H2O,C2H6与NO2反应的化学方程式为4C2H6+14NO2![]() 8CO2+12H2O+7N2。
8CO2+12H2O+7N2。
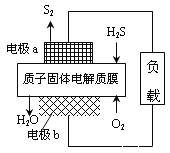
③石墨II通入O2,石墨II为正极,石墨I为负极,Y是一种氧化物,NO2发生氧化反应生成Y,Y为N2O5,电极反应式为NO2-e-+NO3-=N2O5。
(3)应用盖斯定律,将②-①-③得,CH4(g)+CO2(g)=2CO(g)+2H2(g)ΔH=ΔH2-ΔH1-ΔH3。这种方法的推广与使用,不仅实现资源综合利用,而且还能解决的环境问题是:减少温室气体的排放,缓解温室效应。