��Ŀ����
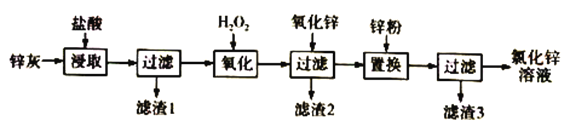
����Ŀ����2 L���ܱ������з�����ӦxA(g)��yB(g) ![]() zC(g)��ͼ�ױ�ʾ200 ��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ�ұ�ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A)��n(B)�ı仯��ϵ�������н�����ȷ���ǣ� ����
zC(g)��ͼ�ױ�ʾ200 ��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ�ұ�ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A)��n(B)�ı仯��ϵ�������н�����ȷ���ǣ� ����
A.200 ��ʱ����Ӧ�ӿ�ʼ��ƽ���ƽ������v(B)��0.04 mol��L��1��min��1
B.200��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ25 L2/mol2
C.�����������200�潵�µ�100�棬ԭƽ��һ�����ƻ��������淴Ӧ���ʾ�����
D.��ͼ�ҿ�֪����ӦxA(g)��yB(g) ![]() zC(g)�Ħ�H<0����a��2
zC(g)�Ħ�H<0����a��2
���𰸡�B
��������A������v= ![]() ��֪v��B��=
��֪v��B��= ![]() molL-1min-1=0.02molL-1min-1����A���������⣻
molL-1min-1=0.02molL-1min-1����A���������⣻
B����ͼ��֪ƽ��ʱA��B��C�����ʵ����ֱ�Ϊ0.4mol��0.2mol��0.2mol���������ǵ�Ũ�ȷֱ�Ϊ��0.2mol/L��0.1mol/L��0.1mol/L����ϻ�ѧ����ʽ2A��g��+B��g�� ![]() C��g������֪�÷�Ӧ��ƽ�ⳣ��Ϊ
C��g������֪�÷�Ӧ��ƽ�ⳣ��Ϊ ![]() L2/mol2=25L2/mol2����B�������⣻
L2/mol2=25L2/mol2����B�������⣻
C������ͼ�ҿ�֪�������¶ȣ�C�������������ƽ�������ƶ�����������ӦΪ���ȷ�Ӧ�����������¶�ƽ�������ƶ���ͬʱ��Ӧ��������C���������⣻
D������ͼ�ҿ�֪�������¶ȣ�C�������������ƽ�������ƶ�����������ӦΪ���ȷ�Ӧ����H��0����Ͷ��ķ�Ӧ������ʵ���֮�ȵ��ڻ�ѧ��Ӧ�м�����֮��ʱ��ƽ��ʱC��������������ֵ�����ݻ�ѧ����ʽ2A��g��+B��g��C��g������֪a=2����D���������⣻
���Դ��ǣ�B
�����㾫����������Ҫ�����˷�Ӧ���ʵĶ�����ʾ�����ͻ�ѧƽ��״̬���ʼ����������֪ʶ�㣬��Ҫ���շ�Ӧ���ʵĵ�λ��mol/(L��min)��mol/(L��s) v=��c-��t����ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч��������ȷ�����⣮

 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�����Ŀ��������(SO2Cl2)���ۺ��Ϻ������Ĥ��ǿ�ҵĴ̼��ԣ������ڹ�ҵ������Ҫ���á���������IJ����������±���
���� | �۵�/�� | �е�/�� | �������� |
SO2Cl2 | -54.1 | 69.1 | ����ˮ��ˮ�⣬����������������������ǿ�� ���ֽ�:SO2Cl2 |
H2SO4 | 10.4 | 338 | ǿ��ˮ�ԡ��ȶ����ֽ� |
ʵ�����ø��﴿�������������Ķ��������ڻ���̿�Ĵ������ºϳ������ȣ���Ӧ����ʽΪ:SO2(g)+Cl2(g)=SO2Cl2(1)H<0����ʵ��װ����ͼ��ʾ(�г�������ʡ��):

(1)����A������Ϊ____________����ȴˮӦ�ô�______(�a����b��)�ڽ��롣
(2)����B��ʢ�ŵ�ҩƷ��__________��
(3)ʵ��ʱ��װ�����з�����Ӧ�Ļ�ѧ����ʽΪ____________��
(4)��ȱ��װ���ҺͶ����������Ȼ�ˮ�⣬������ˮ��Ļ�ѧ����ʽΪ___________��
(5)��Ӧһ��ʱ������ڱ�װ�õ�����ƿ���������ˮԡװ�ã���ԭ����__________��
(6)ʵ�鿪ʼʱ�����п�ʼ����12.25gKC1O3������KC1O3�ڹ���������������ȫת��ΪCl2��ʵ�������õ�32.4g�����������ȣ��������ȵIJ���Ϊ______��
(7)����������Ҳ����믻���(ClSO2OH)ֱ�ӷֽ��ã���Ӧ����ʽΪ:2ClSO2OH=H2SO4+SO2Cl2��
���ڷֽ�����з���������ȵ�ʵ�����������_____����ʵ�����ṩ�IJ���������©�����ձ��������ƾ��ơ���Һ�ܡ���ƿ���÷�������л���Ҫ����IJ���������_____��_____��_____��
�ڷ�����IJ�Ʒ����������������H2SO4�������ʵ�鷽�������Ʒ��������(��ѡ�Լ�:ϡ���ᡢϡ���ᡢBaCl2��Һ������ˮ����ɫʯ����Һ):___________________��