题目内容
【题目】如图所示,烧杯甲中盛有少量液态冰醋酸,烧杯乙中盛有NH4Cl晶体,在烧杯乙中再加入适量氢氧化钡晶体[Ba(OH)2·8H2O],搅拌,可观察到冰醋酸逐渐凝结为固体。下列有关判断正确的是( )

A. NH4Cl与Ba(OH)2·8H2O反应的焓变(ΔH)小于0
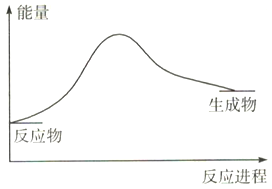
B. 反应物的总能量高于生成物的总能量
C. 反应中有热能转化为产物内部的能量
D. 反应中断裂的化学键只有离子键
【答案】C
【解析】烧杯甲冰醋酸逐渐凝结为固体,说明烧杯乙中的NH4Cl晶体与氢氧化钡晶体[Ba(OH)28H2O]反应吸热,故焓变(ΔH)大于0,反应物的总能量低于生成物的总能量,反应中有热能转化为产物内部的能量,即A、B错误,C正确;D项,NH4Cl晶体与氢氧化钡晶体[Ba(OH)28H2O]反应有BaCl2和NH3H2O生成,既有离子键断裂和生成,又有共价键断裂和生成,D错误。

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
【题目】研究小组进行如下表所示的原电池实验:
实验编号 | ① | ② |
实验装置 |
|
|
实验现象 | 连接好装置5分钟后,灵敏电流计指针向左偏转,两侧铜片表面均无明显现象 | 连接好装置。开始时左侧铁片表面持续产生气泡,5分钟后,灵敏电流计指针向右偏转,右侧铁片表面无明显现象 |
下列关于该实验的叙述中,正确的是
A. 两装置的盐桥中,阳离子均向右侧移动
B. 实验①中,左侧的铜被腐蚀
C. 实验②中,连接装置5分钟后,左侧电极的电极反应式为:2H++2e-=H2↑
D. 实验①和实验②中,均有O2得电子的反应发生