题目内容
【题目】碳、氮广泛的分布在自然界中,碳、氮的化合物性能优良在工业生产和科技领域有重要用途。
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700℃的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g)![]() Si3N4(s)+6CO(g),已知60gSiO2完全反应时放出530.4kJ的能量,则该反应每转移1mole-,可放出的热量为___________________。
Si3N4(s)+6CO(g),已知60gSiO2完全反应时放出530.4kJ的能量,则该反应每转移1mole-,可放出的热量为___________________。
(2)某研究小组现将三组CO(g)与H2O(g)混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g)==CO2(g)+H2(g),得到如下数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
CO | H2O | CO | H2 | |||
1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
2 | 900 | 1 | 2 | 0.5 | 0.5 | |
①实验1中,前5min的反应速率v(H2O)=_____________。
②下列能判断实验2已经达到平衡状态的是______________________。
a.混合气体的密度保持不变 b.容器内CO、H2O、CO2、H2的浓度比不再变化
c.容器内压强不再变化 d..容器中气体的平均相对分子质量不随时间而变化
e. v正(CO)=v逆(H2O)
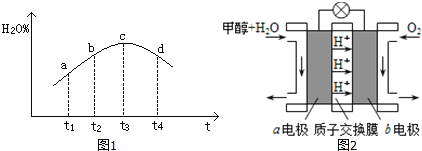
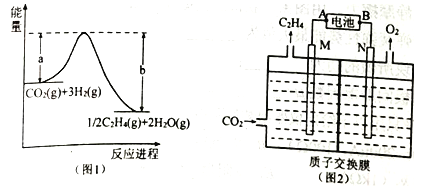
③若实验3的容器是绝热恒容的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如左上图所示,b点v正_________v逆(填“<”、“=”或“>”)
(3)利用CO与H2可直接合成甲醇,右上图是由“甲醇(CH3OH)一空气”形成的绿色燃料电池的工作原理示意图,b电极是该燃料电池的_________(选“正极”或“负极”);写出以石墨为电极的电池工作时负极的电极反应式___________________________________。
【答案】 132.6kJ 0.15mol·L-1·min-1 be > 正极 CH3OH-6e-+H2O=CO2+6H+
【解析】分析:(1)根据方程式3SiO2(s)+6C(s)+2N2(g)![]() Si3N4(s)+6CO(g),可以知道60gSiO2(1molSiO2)完全反应时,转移4mol电子,放出530.4kJ热量,据此计算;
Si3N4(s)+6CO(g),可以知道60gSiO2(1molSiO2)完全反应时,转移4mol电子,放出530.4kJ热量,据此计算;
(2)①根据 计算V(H2),再根据速率之比等于化学计量数之比计算V(H2O);
计算V(H2),再根据速率之比等于化学计量数之比计算V(H2O);
② a.恒容条件下,反应物和产物都是气体,密度始终不变;
b.容器内CO、H2O、CO2、H2的浓度不再变化,则说明反应处于平衡状态;
c.恒温、恒容条件下,气体的总物质的量始终不变,压强始终不变;
d.该反应气体的物质的量不变,气体的质量也不变,所以反应过程中气体的平均相对分子质量不变;
e.V正(CO)=V逆(H2O),转化成H2O的正、逆反应速率相等;
③ c到达平衡,而b点未达到平衡,正反应速率减小,逆反应速率增大至相等,故b点![]() ;
;
(3)通甲醇(CH3OH)的一极为负极,电极的电池工作时负极的电极反应式为CH3OH-6e-+H2O=CO2+6H+。
详解:(1)根据方程式3SiO2(s)+6C(s)+2N2(g)![]() Si3N4(s)+6CO(g),可以知道60gSiO2(1molSiO2)完全反应时,转移4mol电子,放出530.4kJ热量,所以每转移每转移1mole-,可放出的热量为132.6kJ,
Si3N4(s)+6CO(g),可以知道60gSiO2(1molSiO2)完全反应时,转移4mol电子,放出530.4kJ热量,所以每转移每转移1mole-,可放出的热量为132.6kJ,
因此,本题正确答案是:132.6kJ;
(2)① v(H2) =![]() =0.15mol/(L
=0.15mol/(L![]() min),速率之比等于化学计量数之比,则v(H2O)=v(H2)= 0.15mol/(L
min),速率之比等于化学计量数之比,则v(H2O)=v(H2)= 0.15mol/(L![]() min),
min),
因此,本题正确答案是: 0.15mol/(L![]() min);
min);
② a.恒容条件下,反应物和产物都是气体,密度始终不变,故a错误;
b. 容器内CO、H2O、CO2、H2的浓度不再变化,则说明反应处于平衡状态,故b正确;
c.恒温、恒容条件下,气体的总物质的量始终不变,压强始终不变,故c错误;
d.该反应气体的物质的量不变,气体的质量也不变,所以反应过程中气体的平均相对分子质量不变,故d错误;
e.V正(CO)=V逆(H2O),转化成H2O的正、逆反应速率相等,故e正确。
故选:be;
③ c到达平衡,而b点未达到平衡,正反应速率减小,逆反应速率增大至相等,故b点![]() ;
;
因此,本题正确答案是:![]() ;
;
(3)通甲醇(CH3OH)的一极为负极,电极的电池工作时负极的电极反应式为CH3OH-6e-+H2O=CO2+6H+,
因此,本题正确答案是:CH3OH-6e-+H2O=CO2+6H+。

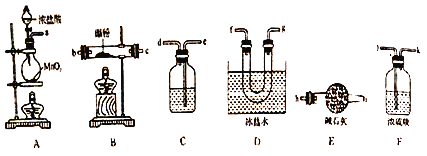
【题目】亚硝酸钠是一种重要的工业用盐,某同学针对亚硝酸钠设计了如下实验:(已知:Na2O2+2NO=2NaNO2;Na2O2+2NO2=2NaNO3)
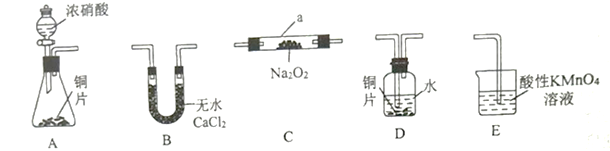
(1)该同学用以上仪器制备NaNO2,则装置的连接顺序为A→___→___→___→___→E。_________(填序号,可重复)
(2)仪器a的名称为______________。
(3)NO在E中可被氧化成NO3-,写出反应的离子方程式_________________________。
(4)比色法测定样品中的NaNO2含量:
①在5个有编号的带刻度试管中分别加入不同量的NaNO2溶液,各加入1mL的M溶液(M遇NaNO2呈紫红色,NaNO2的浓度越大颜色越深),再加蒸馏水至总体积均为10 mL并振荡,制成标准色阶:
试管编号 | a | b | c | d | e |
NaNO2含量/(mg.L-1) | 0 | 20 | 40 | 60 | 80 |
②称量0.10g制得的样品,溶于水配成500mL溶液,取5mL 待测液,加入1mLM溶液,再加蒸馏水至10mL 并振荡,与标准比色阶比较;
③比色的结果是: 待测液的颜色与d 组标准色阶相同,则样品中NaNO2的质量分数为_______。
(5)滴定法测定样品中的NaNO2含量:
①称量0.5000g制得的样品,溶于水配成500mL溶液,取25.00mL待测液于锥形瓶中,加入s mL KI 酸性溶液(足量),发生反应2NO2-+2I-+4H+=2NO↑+I2+2H2O;
②滴入2~3 滴_____作指示剂,用0.0100mol/LNa2S2O3溶液进行滴定,当看到______现象时,即为痛定终点(已知,2 Na2S2O3+ I2=Na2S4O6+2NaI);
③重复实验后,平均消耗Na2S2O3溶液的体积为20.50mL,则样品中NaNO2的质量分数为____(保留3 位有效数字)。
④下列操作会导致测定结果偏高的是______(填序号)。
A.滴定过程中向锥形瓶中加少量水
B.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
C.观察读数时,滴定前仰视,滴定后俯视
D.滴定时摇瓶幅度过大标准溶液滴到瓶外