��Ŀ����
����1.ij�¶�ʱ����2L�ܱ���������X��Y��Z������̬���ʡ�ʵ���ò�ͬʱ�̸����ʵ������±���ʾ��ͬʱ�����3minʱ��������75kJ��
t/min | X/mol | Y/mol | Z/mol |
0 | 1.00 | 1.00 | 0.00 |
3 | 0.75 | 0.50 | 0.50 |
5 | 0.65 | 0.30 | 0.70 |
9 | 0.60 | 0.20 | 0.80 |
14 | 0.60 | 0.20 | 0.80 |
��1��д���÷�Ӧ���Ȼ�ѧ��Ӧ����ʽ�������������������������������� ��
��2�����¶��·�Ӧ��ƽ�ⳣ��K=�������������������� ��
��3�����÷�Ӧ���淴Ӧ������ʱ��Ĺ�ϵ������ͼ��ʾ��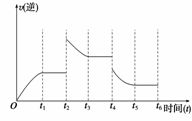 ��
��
�� t2��t3ʱƽ�������� ��������������桱����Ӧ�����ƶ���
�� t4ʱ���ı������������������� (ѡ��һ����ȷѡ��)
A.���¡� B. ���¡��� C.��ѹ�� D.��ȥ���ַ�Ӧ� E.���븺����
������ ����2.����ʵ�飬����þ�����������ڲ�ͬ�¶��·�Ӧ��̽����������Է�Ӧ���ʵ�Ӱ�졣����ʵ���ñ����£�
ʵ�� ��� | �¶�/K | ����Ũ�� /mol��L-1 | ����Ũ��/mol��L-1 | ʵ��Ŀ�� |
�� | 298 | 0.20 | a.ʵ��ٺ͢ڣ�̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죻 b.ʵ��ٺۣ͢�̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죻 c.ʵ��ܢݣ�̽���¶ȶ�þ�����ᷴӦ��þ����ᷴӦ���ʵ�Ӱ�죬�ĸ�����һЩ�� | |
�� | 308 | 0.20 | ||
�� | 298 | 0.40 | ||
�� | 0.20 | 0.20 | ||
�� |
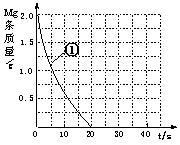 ��4��������Ϲ���������дʵ��ܢݵĿո�
��4��������Ϲ���������дʵ��ܢݵĿո�
��5���ϱ�ʵ����У�þ����ʧ��ʱ��Ϊ20s��ʵ������У�þ
��ʣ��������ʱ���ϵͼ����ͼ��
��. ���跴Ӧ����������������䣬��Ҫ����÷�Ӧ������
v(HCl)����ȱ�ٵ����������������� ��
��.����Ӧ�¶�ÿ����10�棬��Ӧ��������ԭ����2������
����ͬʱ����������ͬŨ������ƽ���ٶȵ�1/2������ͼ
�д��»�����ʵ��ڡ�����ʵ����д���ʵ�顱��þ��������
ʱ���ϵ���ߣ����âڻ��ע�����ߴ�����ʵ�飨����ʵ��������þ��ȫ��ͬ����þ
������ȫ�ܽ⣩��
��1��X(g)+2Y(g) ![]() 2Z(g) ��H =+300 kJ/mol
2Z(g) ��H =+300 kJ/mol
��2��160/3 ����53.3��
��3������ �� B��C
��4���� 298��308���� 308��298��0.20��0.20
��5����. ����������
��. ���ߢڣ����ͬ�٣��յ��ں�����10�������ߢܣ�Ӧ���ݵڢ�С�������д���¶�ȷ������Ϊ298K�����յ��ں�����40������Ϊ308K������������غϣ�ֻҪע��ʵ���ż��ɡ�

 Сѧѧϰ�ð���ϵ�д�
Сѧѧϰ�ð���ϵ�д� Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д���13�֣�����1.ij�¶�ʱ����2L�ܱ���������X��Y��Z������̬���ʡ�ʵ���ò�ͬʱ�̸����ʵ������±���ʾ��ͬʱ�����3minʱ��������75kJ��
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.60 | 0.20 | 0.80 |
| 14 | 0.60 | 0.20 | 0.80 |
��1��д���÷�Ӧ���Ȼ�ѧ��Ӧ����ʽ�� ��
��2�����¶��·�Ӧ��ƽ�ⳣ��K= ?��
��3�����÷�Ӧ���淴Ӧ������ʱ��Ĺ�ϵ����ͼ��ʾ����
�� t2��t3ʱƽ���� ����������桱����Ӧ�����ƶ���
�� t4ʱ���ı����������� (ѡ��һ����ȷѡ��)
A.���� B. ���� C.��ѹ D.��ȥ���ַ�Ӧ�� E.���븺����
����2.����ʵ�飬����þ�����������ڲ�ͬ�¶��·�Ӧ��̽����������Է�Ӧ���ʵ�Ӱ�졣����ʵ���ñ����£�
| ʵ�� ��� | �¶�/K | ����Ũ�� /mol��L-1 | ����Ũ��/mol��L-1 | ʵ��Ŀ�� |
| �� | 298 | 0.20 |
| a.ʵ��ٺ͢ڣ�̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죻 b.ʵ��ٺۣ͢�̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죻 c.ʵ��ܢݣ�̽���¶ȶ�þ�����ᷴӦ��þ����ᷴӦ���ʵ�Ӱ�죬�ĸ�����һЩ�� |
| �� | 308 | 0.20 |
| |
| �� | 298 | 0.40 |
| |
| �� |
| 0.20 | 0.20 | |
| �� |
|
|
|
��4��������Ϲ���������дʵ��ܢݵĿո�
��5���ϱ�ʵ����У�þ����ʧ��ʱ��Ϊ20s��ʵ������У�þ��ʣ��������ʱ���ϵͼ��ͼ��

��. ���跴Ӧ����������������䣬��Ҫ����÷�Ӧ������v(HCl)����ȱ�ٵ������� ��
��.����Ӧ�¶�ÿ����10�棬��Ӧ��������ԭ����2�����¶���ͬʱ����������ͬŨ������ƽ���ٶȵ�1/2������ͼ�д��»�����ʵ��ڡ�����ʵ����д���ʵ�顱��þ��������ʱ���ϵ���ߣ����âڻ��ע�����ߴ�����ʵ�飨����ʵ��������þ��ȫ��ͬ����þ������ȫ�ܽ⣩��
��13�֣�����1.ij�¶�ʱ����2L�ܱ���������X��Y��Z������̬���ʡ�ʵ���ò�ͬʱ�̸����ʵ������±���ʾ��ͬʱ�����3minʱ��������75kJ��
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.60 | 0.20 | 0.80 |
| 14 | 0.60 | 0.20 | 0.80 |
��2�����¶��·�Ӧ��ƽ�ⳣ��K= ?��

��3�����÷�Ӧ���淴Ӧ������ʱ��Ĺ�ϵ����ͼ��ʾ����
�� t2��t3ʱƽ���� ����������桱����Ӧ�����ƶ���
��t4ʱ���ı����������� (ѡ��һ����ȷѡ��)
| A������ | B������ | C����ѹ | D����ȥ���ַ�Ӧ�� E.���븺���� |
| ʵ�� ��� | �¶�/K | ����Ũ�� /mol��L-1 | ����Ũ��/mol��L-1 | ʵ��Ŀ�� |
| �� | 298 | 0.20 | | a.ʵ��ٺ͢ڣ�̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죻 b.ʵ��ٺۣ͢�̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죻 c.ʵ��ܢݣ�̽���¶ȶ�þ�����ᷴӦ��þ����ᷴӦ���ʵ�Ӱ�죬�ĸ�����һЩ�� |
| �� | 308 | 0.20 | | |
| �� | 298 | 0.40 | | |
| �� | | 0.20 | 0.20 | |
| �� | | | |
��5���ϱ�ʵ����У�þ����ʧ��ʱ��Ϊ20s��ʵ������У�þ��ʣ��������ʱ���ϵͼ��ͼ��

��. ���跴Ӧ����������������䣬��Ҫ����÷�Ӧ������v(HCl)����ȱ�ٵ������� ��
��.����Ӧ�¶�ÿ����10�棬��Ӧ��������ԭ����2�����¶���ͬʱ����������ͬŨ������ƽ���ٶȵ�1/2������ͼ�д��»�����ʵ��ڡ�����ʵ����д���ʵ�顱��þ��������ʱ���ϵ���ߣ����âڻ��ע�����ߴ�����ʵ�飨����ʵ��������þ��ȫ��ͬ����þ������ȫ�ܽ⣩��
��14�֣�I��ij�¶�ʱ����һ��2L���ܱ������У� X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ�����д���пհף�

��1���÷�Ӧ�Ļ�ѧ����ʽΪ
��2����Ӧ��ʼ��2min������Z��ƽ����Ӧ����Ϊ
��3����X��Y��Z��Ϊ���壬��Ӧ��ƽ��ʱ����ʱ�����ڵ�ѹǿ����ʼѹǿ֮��Ϊ
II��һ�������£��Ȼ�þ�����Ȼ��ѵĻ�������ϩ���ۺϷ�Ӧ�Ĵ�����Ϊ��̽���¶ȡ��Ȼ�þ����ĺ�ˮ���Լ����鷽ʽ�Ըô�����Ч����Ӱ�죬������¶Ա�ʵ�飺
|
ʵ����� |
�Ȼ�þ��������Ԫ�غ���/% |
�¶�/�� |
���鷽ʽ/ |
����/g��g-1 |
|
1 |
70.97 |
20 |
������ĥ |
3.9��104 |
|
2 |
74.45 |
20 |
������ĥ |
5.0��104 |
|
3 |
74.45 |
20 |
����ĥ |
5.9��104 |
|
4 |
�� |
100 |
����ĥ |
|
ע����Ч���õ�λʱ����ÿ�˴����õ���Ʒ����������ʾ��
��1������= ��
��2����ʵ��1��2���Եó��Ľ����� ��
��3�����ʵ��2��3��Ŀ���� ��
III����������������Ӧ����A��NaOH + HCl = NaCl + H2O
��B��2FeCl3 + Cu = 2FeCl2 + CuCl2
��1����������Ӧ���ʣ��ж��ܷ���Ƴ�ԭ���________________________
��2��������ܣ�˵����ԭ��__________________________
��3��������ԣ���д�������������ϡ��������Һ����______ ____��
��13�֣�����1.ij�¶�ʱ����2L�ܱ���������X��Y��Z������̬���ʡ�ʵ���ò�ͬʱ�̸����ʵ������±���ʾ��ͬʱ�����3minʱ��������75kJ��
|
t/min |
X/mol |
Y/mol |
Z/mol |
|
0 |
1.00 |
1.00 |
0.00 |
|
3 |
0.75 |
0.50 |
0.50 |
|
5 |
0.65 |
0.30 |
0.70 |
|
9 |
0.60 |
0.20 |
0.80 |
|
14 |
0.60 |
0.20 |
0.80 |
��1��д���÷�Ӧ���Ȼ�ѧ��Ӧ����ʽ�� ��
��2�����¶��·�Ӧ��ƽ�ⳣ��K= ?��

��3�����÷�Ӧ���淴Ӧ������ʱ��Ĺ�ϵ����ͼ��ʾ����
�� t2��t3ʱƽ���� ����������桱����Ӧ�����ƶ���
�� t4ʱ���ı����������� (ѡ��һ����ȷѡ��)
A.���� B. ���� C.��ѹ D.��ȥ���ַ�Ӧ�� E.���븺����
����2.����ʵ�飬����þ�����������ڲ�ͬ�¶��·�Ӧ��̽����������Է�Ӧ���ʵ�Ӱ�졣����ʵ���ñ����£�
|
ʵ�� ��� |
�¶�/K |
����Ũ�� /mol��L-1 |
����Ũ��/mol��L-1 |
ʵ��Ŀ�� |
|
�� |
298 |
0.20 |
|
a.ʵ��ٺ͢ڣ�̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죻 b.ʵ��ٺۣ͢�̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죻 c.ʵ��ܢݣ�̽���¶ȶ�þ�����ᷴӦ��þ����ᷴӦ���ʵ�Ӱ�죬�ĸ�����һЩ�� |
|
�� |
308 |
0.20 |
|
|
|
�� |
298 |
0.40 |
|
|
|
�� |
|
0.20 |
0.20 |
|
|
�� |
|
|
|
��4��������Ϲ���������дʵ��ܢݵĿո�
��5���ϱ�ʵ����У�þ����ʧ��ʱ��Ϊ20s��ʵ������У�þ��ʣ��������ʱ���ϵͼ��ͼ��

��. ���跴Ӧ����������������䣬��Ҫ����÷�Ӧ������v(HCl)����ȱ�ٵ������� ��
��.����Ӧ�¶�ÿ����10�棬��Ӧ��������ԭ����2�����¶���ͬʱ����������ͬŨ������ƽ���ٶȵ�1/2������ͼ�д��»�����ʵ��ڡ�����ʵ����д���ʵ�顱��þ��������ʱ���ϵ���ߣ����âڻ��ע�����ߴ�����ʵ�飨����ʵ��������þ��ȫ��ͬ����þ������ȫ�ܽ⣩��