题目内容
【题目】某有机物的结构简式如图所示,下列有关它的性质的叙述中,正确的是
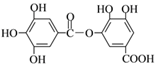
A. 有弱酸性,1 mol该有机物与溴水反应,最多能消耗4 mol Br2
B. 它能发生水解反应,水解后能生成两种产物
C. 在Ni催化下,1 mol该物质可以和7 mol H2发生加成反应
D. 在一定条件下,1 mol该物质最多能与6 mol NaOH完全反应
【答案】A
【解析】该有机物分子中含有羧基,具有酸性,含有酚羟基,邻对位与溴水发生取代反应,碳碳双键与溴水发生加成反应,则1mol该物质消耗溴为4 mol Br2,A正确;酯基水解后生成酸和醇,而产物的结构式相同,只生成一种产物,B错误;酯基不会与氢气发生加成反应,即在Ni催化下,1 mol该物质可以和6mol H2发生加成反应,C错误;该有机物分子中含有羧基,具有酸性,可与氢氧化钠反应,分子中含有酯基,可发生水解,水解产物中含有酚羟基和乙酸,都可与氢氧化钠反应,则1 mol该物质最多能与7 mol NaOH完全反应,D错误;正确选项A。

【题目】硫代硫酸钠晶体(Na2S2O3·5H2O,M=248 g·mol1)可用作定影剂、还原剂。回答下列问题:
(1)已知:Ksp(BaSO4)=1.1×1010,Ksp(BaS2O3)=4.1×105。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
试剂:稀盐酸、稀H2SO4、BaCl2溶液、Na2CO3溶液、H2O2溶液
实验步骤 | 现象 |
①取少量样品,加入除氧蒸馏水 | ②固体完全溶解得无色澄清溶液 |
③___________ | ④___________,有刺激性气体产生 |
⑤静置,___________ | ⑥___________ |
(2)利用K2Cr2O7标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制:称取1.2000 g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在__________中溶解,完全溶解后,全部转移至100 mL的_________中,加蒸馏水至____________。
②滴定:取0.00950 mol·L1的K2Cr2O7标准溶液20.00 mL,硫酸酸化后加入过量KI,发生反应: Cr2O72+6I+14H+![]() 3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32
3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32![]() S4O62+2I。加入淀粉溶液作为指示剂,继续滴定,当溶液__________,即为终点。平行滴定3次,样品溶液的平均用量为24.80 mL,则样品纯度为_________%(保留1位小数)。
S4O62+2I。加入淀粉溶液作为指示剂,继续滴定,当溶液__________,即为终点。平行滴定3次,样品溶液的平均用量为24.80 mL,则样品纯度为_________%(保留1位小数)。

