题目内容
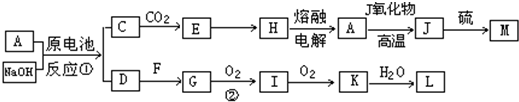
A、J是日常生活中常见的两种金属,这两种金属和NaOH组成原电池,A作负极;F常温下是气体,各物质有以下的转化关系(部分产物及条件略去).
请回答以下问题:
(1)写出下列物质的化学式:M ;L .
(2)写出反应①的化学方程式 .
(3)常温时pH=12的C溶液中,溶质的阳离子与溶质的阴离子浓度之差为 (写出计算式);相同条件下,等浓度的C溶液与CH3COONa溶液中,C的阴离子与CH3COO-浓度的大小关系:前者 后者(用“>”、“<”或“=”表示).
(4)写出反应②的化学方程式 .
(5)含A元素的某盐X常做净水剂,其焰色反应透过蓝色钴玻璃观察为紫色,写出其水溶液与过量的氨水溶液反应的离子方程式为 .

请回答以下问题:
(1)写出下列物质的化学式:M
(2)写出反应①的化学方程式
(3)常温时pH=12的C溶液中,溶质的阳离子与溶质的阴离子浓度之差为
(4)写出反应②的化学方程式
(5)含A元素的某盐X常做净水剂,其焰色反应透过蓝色钴玻璃观察为紫色,写出其水溶液与过量的氨水溶液反应的离子方程式为
分析:A、J是日常生活中常见的两种金属,两种金属和NaOH组成原电池,A作负极,电解质溶液为NaOH,说明A能与氢氧化钠溶液反应,可推知A为Al,故反应①为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,由C→E→H→A→J的转化可知,C为NaAlO2,E为Al(OH)3,H为Al2O3,则D为H2,H→A为工业冶炼金属铝,A→J为铝热反应,故J为Fe、M为FeS.F常温下是气体,与氢气化合生成G,G能连续氧化生成K,K与水反应生成L,中学中只有N元素单质化合物符合,可推知F为N2,G为NH3,I为NO,J为NO2,L为HNO3,据此解答.
解答:解:A、J是日常生活中常见的两种金属,两种金属和NaOH组成原电池,A作负极,电解质溶液为NaOH,说明A能与氢氧化钠溶液反应,可推知A为Al,故反应①为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,由C→E→H→A→J的转化可知,C为NaAlO2,E为Al(OH)3,H为Al2O3,则D为H2,H→A为工业冶炼金属铝,A→J为铝热反应,故J为Fe、M为FeS.F常温下是气体,与氢气化合生成G,G能连续氧化生成K,K与水反应生成L,中学中只有N元素单质化合物符合,可推知F为N2,G为NH3,I为NO,J为NO2,L为HNO3,
(1)由上述分析可知,M为FeS,L为HNO3,故答案为:FeS;HNO3;
(2)反应①的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(3)常温时pH=12的NaAlO2溶液中,根据电荷守恒可知,c(Na+)+c(H+)=c(AlO2-)+c(OH-),则c(Na+)-c(AlO2-)=c(OH-)-c(H+)=(10-2-10-12)mol/L;
相同条件下,等浓度的NaAlO2溶液与CH3COONa溶液中,由于醋酸的酸性比偏铝酸强,故AlO2-的水解程度比CH3COO-水解程度大,溶液中c(AlO2-)<c(CH3COO-),
故答案为:(10-2-10-12)mol/;<;
(4)反应②是氨的催化氧化,反应生成NO与水,反应方程式为:4NH3+5O2
4NO+6H2O,
故答案为:4NH3+5O2
4NO+6H2O;
(5)含Al元素的某盐X常做净水剂,其焰色反应透过蓝色钴玻璃观察为紫色,为KAl(SO4)2,其水溶液与过量的氨水溶液反应生成氢氧化铝沉淀与硫酸铵,反应离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+.
(1)由上述分析可知,M为FeS,L为HNO3,故答案为:FeS;HNO3;
(2)反应①的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(3)常温时pH=12的NaAlO2溶液中,根据电荷守恒可知,c(Na+)+c(H+)=c(AlO2-)+c(OH-),则c(Na+)-c(AlO2-)=c(OH-)-c(H+)=(10-2-10-12)mol/L;
相同条件下,等浓度的NaAlO2溶液与CH3COONa溶液中,由于醋酸的酸性比偏铝酸强,故AlO2-的水解程度比CH3COO-水解程度大,溶液中c(AlO2-)<c(CH3COO-),
故答案为:(10-2-10-12)mol/;<;
(4)反应②是氨的催化氧化,反应生成NO与水,反应方程式为:4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
(5)含Al元素的某盐X常做净水剂,其焰色反应透过蓝色钴玻璃观察为紫色,为KAl(SO4)2,其水溶液与过量的氨水溶液反应生成氢氧化铝沉淀与硫酸铵,反应离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+.
点评:本题考查无机物推断,涉及Al、Fe、N元素单质化合物的转化关系,难度不大,注意基础知识的全面掌握.

练习册系列答案
相关题目
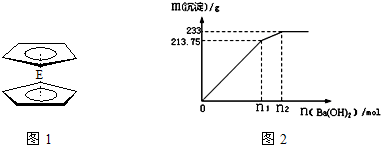
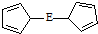 .核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有
.核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有