题目内容
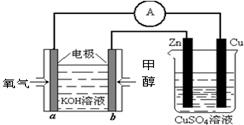
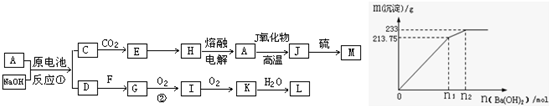
(2012?上饶一模)如图1,A、J是日常生活中常见的两种金属,这两种金属和NaOH组成原电池,A作负极;F常温下是气体,各物质有以下的转化关系(部分产物及条件略去).
请回答以下问题:
(1)写出原电池的负极反应方程式
(2)常温时pH=12的C溶液中,溶质的阳离子与溶质的阴离子浓度之差为
(3)金属A的氯化物沸点较低,又易升华,能否电解这种熔融氯化物来生产A?
(4)写出②的化学方程式
(5)写出A→J反应的化学方程式
(6)含A元素的某盐X常做净水剂,X做焰色反应时,透过钴玻璃观察火焰呈紫色.则:
①水溶液与NaHCO3溶液混合,反应的离子方程式为:
②500mLX的溶液与Ba(OH)2反应生成沉淀的质量与加入Ba(OH)2物质的量的关系如图2:请回答:X晶体的俗名为

请回答以下问题:
(1)写出原电池的负极反应方程式
Al+4OH--3e-=AlO2-+2H2O
Al+4OH--3e-=AlO2-+2H2O
.(2)常温时pH=12的C溶液中,溶质的阳离子与溶质的阴离子浓度之差为
10-2-10-12mol/L或c(OH-)-c(H+)
10-2-10-12mol/L或c(OH-)-c(H+)
(写出计算式);相同条件下,等浓度的C溶液与CH3COONa溶液中,C的阴离子与CH3COO-浓度的大小关系:前者<
<
后者(用“>”、“<”或“=”表示).(3)金属A的氯化物沸点较低,又易升华,能否电解这种熔融氯化物来生产A?
否
否
.原因是因为A的氯化物熔沸点低,据此判断它的晶体为分子晶体,在熔融态时不电离,不能被电解
因为A的氯化物熔沸点低,据此判断它的晶体为分子晶体,在熔融态时不电离,不能被电解
.(4)写出②的化学方程式
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
(5)写出A→J反应的化学方程式
Fe2O3+2Al
2Fe+Al2O3
| ||
Fe2O3+2Al
2Fe+Al2O3
.
| ||
(6)含A元素的某盐X常做净水剂,X做焰色反应时,透过钴玻璃观察火焰呈紫色.则:
①水溶液与NaHCO3溶液混合,反应的离子方程式为:
Al3++3HCO3-=Al(OH)3↓+3CO2↑
Al3++3HCO3-=Al(OH)3↓+3CO2↑
②500mLX的溶液与Ba(OH)2反应生成沉淀的质量与加入Ba(OH)2物质的量的关系如图2:请回答:X晶体的俗名为
明矾或白矾
明矾或白矾
;其溶液的物质的量浓度为1mol/L
1mol/L
mol/L.分析:(1)题中C→E→H→A→J的转化是中学化学中常见反应,H→A为工业冶炼金属铝,A→J为铝热反应,故应为AlO2-→Al(OH)3→Al2O3→Al→Fe的反应,该原电池是铝做负极,铁做正极,电解质溶液为NaOH,负极上发生的反应为:
Al+4OH--3e-=AlO2-+2H2O;
(2)溶液C为NaAlO2,根据溶液呈电中性,即c(AlO2-)+c(OH-)=c(Na+)+c(H+),进行判断离子关系;
(3)根据AlCl3为共价化合物在熔融状态下不导电进行分析;
(4)反应②为工业合成氨的重要反应,反应为:4NH3+5O2
4NO+6H2O;
(5)反应A→J为铝热反应,反应为:Fe2O3+2Al
2Fe+Al2O3;
(6)①根据弱酸的阴离子和弱碱的阳离子发生相互促进的水解来书写离子方程式;
②含A元素的某盐X常做净水剂,X做焰色反应时,透过钴玻璃观察火焰呈紫色,说明盐中含有铝元素和钾元素,为明矾,根据图象判断反应的物质的量的关系,以此计算.
Al+4OH--3e-=AlO2-+2H2O;
(2)溶液C为NaAlO2,根据溶液呈电中性,即c(AlO2-)+c(OH-)=c(Na+)+c(H+),进行判断离子关系;
(3)根据AlCl3为共价化合物在熔融状态下不导电进行分析;
(4)反应②为工业合成氨的重要反应,反应为:4NH3+5O2
| ||
| △ |
(5)反应A→J为铝热反应,反应为:Fe2O3+2Al
| ||
(6)①根据弱酸的阴离子和弱碱的阳离子发生相互促进的水解来书写离子方程式;
②含A元素的某盐X常做净水剂,X做焰色反应时,透过钴玻璃观察火焰呈紫色,说明盐中含有铝元素和钾元素,为明矾,根据图象判断反应的物质的量的关系,以此计算.
解答:解:(1)题中H→A为工业冶炼金属铝,A→J为铝热反应,为推断题的突破口,依次可知C→E→H→A→J的转化是中学化学中常见反应,为AlO2-→Al(OH)3→Al2O3→Al→Fe之间的转化,该原电池是铝做负极,铁做正极,电解质溶液为NaOH,可以推知:A为Al,C为NaAlO,E为Al(OH)3,H为Al2O3,J为Fe,M为FeS,原电池中,Al做负极被氧化,在碱性溶液中生成AlO2-,电极反应式为:Al+4OH--3e-=AlO2-+2H2O,故答案为:Al+4OH--3e-=AlO2-+2H2O;
(2)溶液C为NaAlO2,根据溶液呈电中性,即c(AlO2-)+c(OH-)=c(Na+)+c(H+)可知:c(Na+)-c(AlO2-)=c(OH-)-c(H+)=10-2-10-12 mol/L,故答案为:10-2-10-12 mol/L或c(OH-)-c(H+);
(3)金属A的氯化物为AlCl3,为共价化合物在熔融状态下不导电,故答案为:否;因为A的氯化物熔沸点低,据此判断它的晶体为分子晶体,在熔融态时不电离,不能被电解;
(4)原电池正极生成H2,即D为H2,则G为氢化物,由G→I→K的转化可知该氢化物中存在变价非金属元素,应为N元素,故G为NH3,I为NO,K为NO2,L为HNO3,反应②为工业合成氨的重要反应,反应为:4NH3+5O2
4NO+6H2O,
故答案为:4NH3+5O2
4NO+6H2O
(5)反应A→J为铝热反应,反应为:Fe2O3+2Al
2Fe+Al2O3 故答案为:Fe2O3+2Al
2Fe+Al2O3
(6)①AlCl3水溶液与NaHCO3溶液反应相互促进的水解,反应为Al3++3HCO3-=Al(OH)3↓+3CO2↑,该反应为泡沫灭火器的反应原理,故答案为:Al3++3HCO3-=Al(OH)3↓+3CO2↑;
②含A元素的某盐X常做净水剂,X做焰色反应时,透过钴玻璃观察火焰呈紫色,说明盐中含有铝元素和钾元素,为明矾,俗称为明矾或白矾;
根据反应计算:
Ba2++SO42-═BaSO4
1mol 233g
n 233g
则n=1mol,根据SO42-离子的守恒可知500mLKAl(SO4)2的溶液中含有溶质的物质的量为0.5mol,
故浓度为:
=1mol/L,故答案为:明矾或白矾;1mol/L.
(2)溶液C为NaAlO2,根据溶液呈电中性,即c(AlO2-)+c(OH-)=c(Na+)+c(H+)可知:c(Na+)-c(AlO2-)=c(OH-)-c(H+)=10-2-10-12 mol/L,故答案为:10-2-10-12 mol/L或c(OH-)-c(H+);
(3)金属A的氯化物为AlCl3,为共价化合物在熔融状态下不导电,故答案为:否;因为A的氯化物熔沸点低,据此判断它的晶体为分子晶体,在熔融态时不电离,不能被电解;
(4)原电池正极生成H2,即D为H2,则G为氢化物,由G→I→K的转化可知该氢化物中存在变价非金属元素,应为N元素,故G为NH3,I为NO,K为NO2,L为HNO3,反应②为工业合成氨的重要反应,反应为:4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
(5)反应A→J为铝热反应,反应为:Fe2O3+2Al
| ||
| ||
(6)①AlCl3水溶液与NaHCO3溶液反应相互促进的水解,反应为Al3++3HCO3-=Al(OH)3↓+3CO2↑,该反应为泡沫灭火器的反应原理,故答案为:Al3++3HCO3-=Al(OH)3↓+3CO2↑;
②含A元素的某盐X常做净水剂,X做焰色反应时,透过钴玻璃观察火焰呈紫色,说明盐中含有铝元素和钾元素,为明矾,俗称为明矾或白矾;
根据反应计算:
Ba2++SO42-═BaSO4
1mol 233g
n 233g
则n=1mol,根据SO42-离子的守恒可知500mLKAl(SO4)2的溶液中含有溶质的物质的量为0.5mol,
故浓度为:
| 0.5mol |
| 0.5L |
点评:本题考查元素化合物推断,同时考查电化学、晶体类型的判断、盐类的水解等知识,具有较高的综合度,本题具有一定的难度.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目


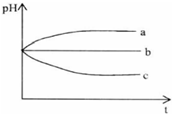 (2012?上饶一模)将pH相同的三种酸性溶液露置于空气中一段时间后,溶液的pH随时间的变化情况如图所示:则a、b、c三种溶液分别可能为( )
(2012?上饶一模)将pH相同的三种酸性溶液露置于空气中一段时间后,溶液的pH随时间的变化情况如图所示:则a、b、c三种溶液分别可能为( )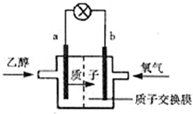 (2012?上饶一模)乙醇燃料电池中采用磺酸类质子溶剂,电池总反应为:C2H5OH+3O2=2CO2+3H2O下列说法错误的是( )
(2012?上饶一模)乙醇燃料电池中采用磺酸类质子溶剂,电池总反应为:C2H5OH+3O2=2CO2+3H2O下列说法错误的是( )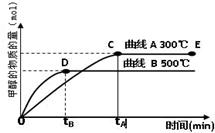 (2012?上饶一模)能源问题是人类社会面临的重大课题,日本大地震引起的核泄漏事故引起了人们对核能源的恐慌.而甲醇是未来重要的绿色能源之一.
(2012?上饶一模)能源问题是人类社会面临的重大课题,日本大地震引起的核泄漏事故引起了人们对核能源的恐慌.而甲醇是未来重要的绿色能源之一. CH3OH(g).甲醇的物质的量与反应温度的关系如图所示:
CH3OH(g).甲醇的物质的量与反应温度的关系如图所示: