题目内容
某无色气体可能含有HCl、 HBr 、SO2 、CO2 中的一种或几种。将气体通入到适量氯水中,恰好完全反应,不再剩余气体。将所得的无色溶液分装在两个试管中,分别加入酸化的AgNO3 溶液和酸化的BaCl2溶液,均产生白色沉淀。则下列判断正确的是( )
A.原气体中一定有SO2 ,一定无HBr B.原气体中可能有SO2
C.原气体中一定有HCl D.不能确定有无HCl,但一定无CO2
A、D
解析:
此题考查元素化合物知识,重要的是熟悉氯水的氧化性,熟悉相关的反应规律,还要明确相关物质的转化关系,这是分析问题的基础。将气体通入氯水中无气体剩余,说明一定无CO2 ;所得溶液无色,说明无HBr(溴水为橙黄色);再加入AgNO3溶液和BaCl2均得白色沉淀,说明含SO2 (因为SO2+Cl2+2H2O=H2SO4 +2HCl),至于HCl气体则无法判断。

练习册系列答案
相关题目
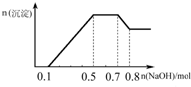 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味无毒的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀的物质的量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味无毒的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀的物质的量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )| A、溶液中的阳离子只有H+、Mg2+、Al3+ | B、溶液中n(NH4+)=0.2mol | C、溶液中一定不含CO32-,可能含有SO42-和NO3- | D、三种离子的物质的量之比n(H+):n(Al3+):n(Mg2+)=1:1:1 |
 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )

