题目内容
NA为阿伏加德罗常数,下列说法正确的是
| A.1Llmol/L的Na2CO3溶液中含有的CO32-数目为NA |
| B.1 mol羟基(-OH)所含的电子数约为l0NA |
| C.1 mol丙烯分子有2 mol σ 键,1 mol π 键 |
| D.现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
D
解析试题分析:由于Na2CO3是强碱弱酸盐,在溶液中会发生水解反应,所以1Llmol/L的Na2CO3溶液中含有的CO32-数目小于NA,错误;B.1 mol羟基(-OH)所含的电子数约为9NA,错误;C.在丙烯CH2=CHCH3的分子中含有8个σ 键个1 个 π 键,所以1 mol丙烯分子有8mol σ 键,1 mol π 键,错误;D.乙烯、丙烯、丁烯的最简式是CH2,式量是14,所以乙烯、丙烯、丁烯的混合气体共14g,含有1mol的最简式,因此其原子数为3NA,正确。
考点:考查阿伏加德罗常数的计算的知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
把7.4 g Na2CO3·10H2O和NaHCO3组成的固体混合物溶于水配成100 mL溶液,其中c(Na+)="0.6" mol·L-1。若把等质量的固体混合物加热至恒重,残留固体的质量是( )
| A.3.18 g | B.2.12 g | C.4.22 g | D.5.28 g |
下列各项中表达正确的是( )
A.F-的结构示意图: | B.CO2的分子模型示意图: |
C.CSO的电子式: | D.N2的结构式::N≡N: |
设NA为阿伏加德罗常数,下列说法正确的是
| A.若C2H6分子中含共价键数为7NA,则乙烷的体积为22.4L |
| B.58.5g氯化钠固体中含NaCl分子数为NA |
| C.78g液态苯分子中含碳碳双键数目为3NA |
| D.28gN2和6gH2在高温高压铁触媒催化作用下,生成的NH3分子数一定小于2NA |
用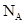 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
A. 中含有的原子数为 中含有的原子数为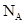 |
B. 中含有的氢原子数为2 中含有的氢原子数为2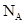 |
C.常温常压下,11.2L 中含有的分子数为0.5 中含有的分子数为0.5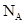 |
D.1L0.1mol·L-1NaNO3溶液中含有的钠离子数为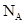 |
下列化学用语对应正确的是
A.CH4分子的比例模型: | B.CCl4的电子式: |
| C.H2O2的结构式:H-O-O-H | D.乙酸的最简式:C2H4O2 |
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A.常温下,23g NO2含有NA个氧原子 |
| B.1L 0.1mol·L-1的氨水含有0.1NA个OH- |
| C.常温常压下,22.4LCCl4含有个NA个CCl4分子 |
| D.1molFe2+ 与足量的H2O2溶液反应,转移2NA个电子 |
下列有关化学用语表示正确的是( )
A.甲基的电子式: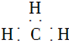 |
B.镁离子的结构示意图: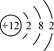 |
C.质量数为34、中子数为18的核素: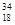 S S |
D.乙酸的结构简式: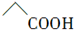 |
NA表示阿伏加德罗常数的值。下列叙述中不正确的是( )
| A.1mol乙烯与乙醇的混合物在氧气中充分燃烧,消耗氧气的分子数为一定为3NA |
| B.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA |
| C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA |
| D.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2 NA |