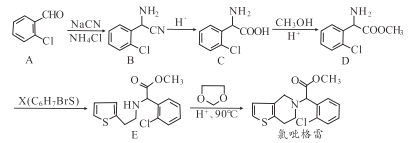
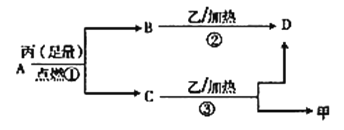
题目内容
【题目】常温下,下列有关电解质溶液的叙述正确的是
A. pH=2的盐酸与pH=12的氨水等体积混合后所得溶液显中性
B. 等浓度等体积的强酸与强碱溶液混合后,溶液的pH=7
C. pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合后溶液的pH=10.7(已知lg2=0.3)
D. 将l0 mL pH=a的盐酸与l00 mL pH=b的Ba(OH)2溶液混合后恰好中和,则a+b=13
【答案】D
【解析】A、氨水为弱碱,溶液中部分电离,则pH=2的盐酸与pH=12的氨水等体积混合后氨水过量,溶液显示碱性,选项A错误;B、强酸强碱混合溶液的酸碱性不仅取决于酸碱的物质的量还取决于酸和碱的元数,如等浓度等体积的盐酸与氢氧化钡溶液混合后,溶液的pH>7,选项B错误;C、混合溶液中c(OH-)=![]() ,c(H+)=
,c(H+)=![]() mol/L=2×10-13mol/L,pH=12.7,选项C错误;D、氯化氢和氢氧化钡都是强电解质,酸碱恰好中和,则盐酸中n(H+)等于氢氧化钡中n(OH-),所以10-a mol/L×0.01L=1014-b mol/L×0.1L,则a+b=13,选项D正确。答案选D。
mol/L=2×10-13mol/L,pH=12.7,选项C错误;D、氯化氢和氢氧化钡都是强电解质,酸碱恰好中和,则盐酸中n(H+)等于氢氧化钡中n(OH-),所以10-a mol/L×0.01L=1014-b mol/L×0.1L,则a+b=13,选项D正确。答案选D。

【题目】在2L密闭容器中,800℃时反应2NO(g)+O2(g)2NO2(g)△H<0,体系中,n(NO)随时间的变化如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)能说明该反应已经达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内物质的密度保持不变
(2)图中表示NO2的变化的曲线是 , 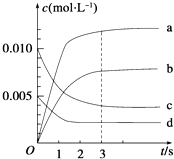
(3)用O2的浓度变化表示从0~2s内该反应的平均速率v= .
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.将容器体积变为1Lb.适当升高温度c.增大O2的浓度d.选择高效的催化剂.