题目内容
【题目】氯化铁在现代生产和生活中应用广泛。某化学研究性学习小组模拟工业生产流程制备无水氯化铁并对产物做了如下探究实验。

经查阅资料得知:①无水氯化铁在空气中易潮解,加热易升华;②工业上,向500—600℃的铁屑中通入氯气可生产无水氯化铁;③向炽热铁屑中通入氯化氢可以生产无水氯化亚铁和氢气。
请回答下列问题:
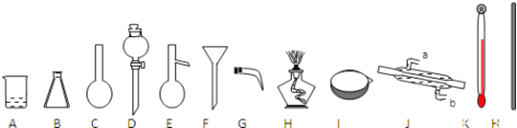
(1)装置的连接顺序为_______________(用a、b、c…h表示)。
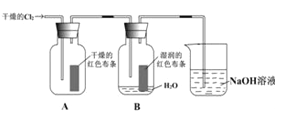
(2)若缺少装置E对本实验造成的影响是________________________。
(3)工业生产中,会将D中干燥剂换成无水氯化钙,通过D后产生的过量氯气再用氯化亚铁溶液吸收,得到氯化铁溶液作为副产品。氯化亚铁溶液因吸收C12失去作用而失效,下列试剂中能够检验氯化亚铁溶液是否完全失效的是_______________。
a.硫氰酸钾溶液 b.铁氰化钾溶液 c.高锰酸钾溶液 d.烧碱溶液
(4)实验结束并冷却后,将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:

淡红色溶液中加入过量H2O2后溶液红色加深的原因是___________________(用离子方程式表示)。
已知红色褪去的同时有气体生成,经检验为O2。该小组对红色褪去的原因进行探究。

根据实验现象判断,以下说法正确的是_________________________。(填标号)
a.实验I说明是SCN发生了反应而不是Fe3+发生反应
b.实验I说明是Fe3+发生了反应而不是SCN-发生反应
c.实验I中第3份溶液中生成的白色沉淀为BaSO3
d.实验Ⅱ排除H2O2分解产生的O2氧化SCN-的可能
由实验I和Ⅱ得出结论为_______________________________________。
【答案】(1)aghdebcf;
(2)防止生成H2与Cl2混合受热发生爆炸;(3)b;
(4)①2Fe2++2H++H2O2=2Fe3++2H2O;②ad,H2O2将SCN-氧化成SO42-。
【解析】
试题分析:(1)首先制备氯气,氯气中混有氯化氢和水蒸气,氯化氢和铁反应,干扰实验,根据信息,氯化铁易潮解,因此先除去氯化氢(用饱和食盐水)、再除去水(用浓硫酸),得到干净的氯气,再和铁反应,氯气有毒,防止污染空气,必须尾气处理,同时防止空气水蒸气进入,因此连接顺序是:a g h d e b c f ;(2)根据信息③铁高温下和氯化氢反应生成氯化亚铁和氢气,氢气和氯气混合反应发生爆炸,因此缺少E装置防止生成H2与Cl2混合受热发生爆炸;(3)氯气把FeCl2氧化成FeCl3,完全失效,说明溶液不存在Fe2+,因此检验Fe2+,Fe2+具有还原性,能使酸性高锰酸钾溶液褪色,但溶液中含有Cl-,也能使酸性高锰酸钾溶液褪色,因此使用铁氰化钾溶液,出现蓝色沉淀,说明含有Fe2+,没有蓝色沉淀产生,说明FeCl2完全失效,故选项b正确;(4)① Fe3++3SCN-![]() Fe(SCN)3,颜色加深,说明反应向正反应方向进行,说明过氧化氢把Fe2+氧化成Fe3+,促使平衡向正反应方向移动,离子反应方程式为:2Fe2++2H++H2O2 = 2Fe3++2H2O;②a、根据实验1的第二份,加入KSCN溶液后,溶液又变红,说明溶液中含有Fe3+,第三份中加入稀盐酸和BaCl2有白色沉淀产生,说明溶液中有SO42-,SCN-被氧化,故正确;b、根据选项a的分析,故错误;c、滴加盐酸,排除或除去SO32-干扰,出现白色沉淀,此沉淀为BaSO4,故错误;d、通入氧气,无现象发生,说明是氧气的缘故,故正确。
Fe(SCN)3,颜色加深,说明反应向正反应方向进行,说明过氧化氢把Fe2+氧化成Fe3+,促使平衡向正反应方向移动,离子反应方程式为:2Fe2++2H++H2O2 = 2Fe3++2H2O;②a、根据实验1的第二份,加入KSCN溶液后,溶液又变红,说明溶液中含有Fe3+,第三份中加入稀盐酸和BaCl2有白色沉淀产生,说明溶液中有SO42-,SCN-被氧化,故正确;b、根据选项a的分析,故错误;c、滴加盐酸,排除或除去SO32-干扰,出现白色沉淀,此沉淀为BaSO4,故错误;d、通入氧气,无现象发生,说明是氧气的缘故,故正确。

 小题狂做系列答案
小题狂做系列答案