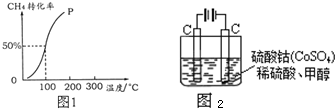
题目内容
某中学的化学兴趣小组对SO2与漂白粉的反应进行实验探究,实验过程如下:取10克漂白粉固体,加入250mL水中,部分固体溶解溶液略有颜色,过滤后用洁净的玻璃棒沾取滤液到pH试纸上,发现pH试纸先变蓝(约为12)后褪色.回答下列问题:
(1)工业制取漂白粉的化学方程式是 ,
漂白粉在空气中变质的原因 (用化学反应方程式说明)
(2)pH试纸颜色的变化说明漂白粉溶液具有的性质是 ,ClO2和漂白粉一样也具有强氧化性,其消毒效率(以单位物质的量得电子的数目表示)是Cl2的 倍;
(3)将SO2持续通入漂白粉溶液中,发现澄清透明的溶液先变为黄绿色,随后溶液中产生大量白色沉淀且黄绿色褪去.回答下列问题:
①澄清透明溶液变为黄绿色的可能原因是:随溶液酸性的增强,漂白粉的有效成分和C1-发生反应.通过进一步实验确认了这种可能性,其实验方案是 ;
②用离子方程式解释现象中黄绿色褪去的原因: ;
③SO2与漂白粉的有效成分在酸性条件下反应的离子方程式: .
(1)工业制取漂白粉的化学方程式是
漂白粉在空气中变质的原因
(2)pH试纸颜色的变化说明漂白粉溶液具有的性质是
(3)将SO2持续通入漂白粉溶液中,发现澄清透明的溶液先变为黄绿色,随后溶液中产生大量白色沉淀且黄绿色褪去.回答下列问题:
①澄清透明溶液变为黄绿色的可能原因是:随溶液酸性的增强,漂白粉的有效成分和C1-发生反应.通过进一步实验确认了这种可能性,其实验方案是
②用离子方程式解释现象中黄绿色褪去的原因:
③SO2与漂白粉的有效成分在酸性条件下反应的离子方程式:
考点:二氧化硫的化学性质,氯气的化学性质
专题:元素及其化合物
分析:(1)氯气与石灰乳制备漂粉,漂白粉在空气中与二氧化碳、水反应生成HClO可变质;
(2)pH试纸先变蓝(约为12)后褪色,则溶液具有碱性、漂白性;利用电子转移计算消毒效率;
(3)SO2持续通入漂白粉溶液中,发现澄清透明的溶液先变为黄绿色,随后溶液中产生大量白色沉淀且黄绿色褪去,黄绿色气体为氯气,白色沉淀为硫酸钙,
①溶液酸性的增强,漂白粉的有效成分和C1-发生反应,则需要加酸;
②氯气与二氧化硫反应;
③SO2与漂白粉的有效成分在酸性条件下,发生氧化还原反应.
(2)pH试纸先变蓝(约为12)后褪色,则溶液具有碱性、漂白性;利用电子转移计算消毒效率;
(3)SO2持续通入漂白粉溶液中,发现澄清透明的溶液先变为黄绿色,随后溶液中产生大量白色沉淀且黄绿色褪去,黄绿色气体为氯气,白色沉淀为硫酸钙,
①溶液酸性的增强,漂白粉的有效成分和C1-发生反应,则需要加酸;
②氯气与二氧化硫反应;
③SO2与漂白粉的有效成分在酸性条件下,发生氧化还原反应.
解答:
解:(1)利用氢氧化钙和氯气发生反应生成次氯酸钙、氯化钙和水,反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉在空气中与二氧化碳、水反应生成HClO可变质,发生的反应为Ca(ClO)2+CO2+H2O=CaCO3+2HClO,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;Ca(ClO)2+CO2+H2O=CaCO3+2HClO;
(2)pH试纸先变蓝(约为12)后褪色,则溶液具有碱性、漂白性;ClO2和漂白粉一样也具有强氧化性,其消毒效率(以单位物质的量得电子的数目表示)是Cl2的
=2.5倍,故答案为:碱性和漂白性;2.5;
(3)SO2持续通入漂白粉溶液中,发现澄清透明的溶液先变为黄绿色,随后溶液中产生大量白色沉淀且黄绿色褪去,黄绿色气体为氯气,白色沉淀为硫酸钙,
①进一步实验确认了这种可能性,其实验方案是向漂白粉溶液中逐滴滴入硫酸,观察溶液颜色是否变为黄绿色,故答案为:向漂白粉溶液中逐滴滴入硫酸,观察溶液颜色是否变为黄绿色;
②用离子方程式解释现象中黄绿色褪去的原因为Cl2+SO2+2H2O=4H++2Cl-+SO42-,故答案为:Cl2+SO2+2H2O=4H++2Cl-+SO42-;
③SO2与漂白粉的有效成分在酸性条件下反应的离子方程式为2SO2+Ca2++2ClO-+2H2O=4H++2Cl-+CaSO4↓+SO42-,故答案为:2SO2+Ca2++2ClO-+2H2O=4H++2Cl-+CaSO4↓+SO42-.
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;Ca(ClO)2+CO2+H2O=CaCO3+2HClO;
(2)pH试纸先变蓝(约为12)后褪色,则溶液具有碱性、漂白性;ClO2和漂白粉一样也具有强氧化性,其消毒效率(以单位物质的量得电子的数目表示)是Cl2的
| 1mol×[4-(-1)] |
| 1mol×2×[0-(-1)] |
(3)SO2持续通入漂白粉溶液中,发现澄清透明的溶液先变为黄绿色,随后溶液中产生大量白色沉淀且黄绿色褪去,黄绿色气体为氯气,白色沉淀为硫酸钙,
①进一步实验确认了这种可能性,其实验方案是向漂白粉溶液中逐滴滴入硫酸,观察溶液颜色是否变为黄绿色,故答案为:向漂白粉溶液中逐滴滴入硫酸,观察溶液颜色是否变为黄绿色;
②用离子方程式解释现象中黄绿色褪去的原因为Cl2+SO2+2H2O=4H++2Cl-+SO42-,故答案为:Cl2+SO2+2H2O=4H++2Cl-+SO42-;
③SO2与漂白粉的有效成分在酸性条件下反应的离子方程式为2SO2+Ca2++2ClO-+2H2O=4H++2Cl-+CaSO4↓+SO42-,故答案为:2SO2+Ca2++2ClO-+2H2O=4H++2Cl-+CaSO4↓+SO42-.
点评:本题考查二氧化硫和氯气的化学性质,为高频考点,综合考查元素化合物知识,把握物质的性质、实验设计及现象与结论的关系为解答的关键,侧重分析与实验能力的综合考查,题目难度不大.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案
相关题目
对于反应3Cl2+6NaOH═5NaCl+NaClO3+3H2O,以下叙述不正确的是( )
| A、NaClO3中Cl的化合价是+5 |
| B、被氧化的Cl原子和被还原的Cl原子的物质的量的比为1:5 |
| C、Cl2既是氧化剂又是还原剂 |
| D、每生成1mol的NaClO3转移6mol的电子 |
 浙江大学的科研小组成功研制出能在“数分钟之内”将电量充满的锂电池,其成本只有传统锂电池的一半.他们把锂锰氧化物(LMO)浸泡在石墨里面,使其变成一个可以导电的密集网络的负极材料(如图),与电解质和正极材料(石墨)构成可充电电池.若电解液为LiAlCl4-SOCl2,电池的总反应为:4LiCl+S+SO2
浙江大学的科研小组成功研制出能在“数分钟之内”将电量充满的锂电池,其成本只有传统锂电池的一半.他们把锂锰氧化物(LMO)浸泡在石墨里面,使其变成一个可以导电的密集网络的负极材料(如图),与电解质和正极材料(石墨)构成可充电电池.若电解液为LiAlCl4-SOCl2,电池的总反应为:4LiCl+S+SO2 | 充电 |
| 放电 |
| A、电池的电解液可为LiCl水溶液 |
| B、该电池放电时,负极发生还原反应 |
| C、充电时阳极反应式为:4Cl-+S+SO2-4e-═2SOCl2 |
| D、放电时电子从负极经外电路流向正极,再从正极经电解质流向负极 |
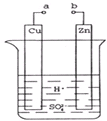 原电池是化学对人类的一项重大贡献.
原电池是化学对人类的一项重大贡献.