题目内容
【题目】MnO2是制造干电池的主要原料之一,也是中学化学中常见的一种试剂。工业上Mn(NO3)2和KMnO4为原料制备MnO2,其生产原理如下:用软锰矿(含MnO2和少量的Fe2O3、SiO2)和碳反应制得MnO;再将MnO与稀硝酸反应,反应后经过滤、提纯、浓缩,可制得50%的Mn(NO3)2溶液;在一定条件下,把50%的Mn(NO3)2溶液滴加到KMnO4溶液中,发生如下反应:3Mn(NO3)2+2KMnO4+2H2O═5MnO2↓+2KNO3+4HNO3,反应生成的沉淀经过滤、洗涤、干燥后得到MnO2。
请回答下列问题:
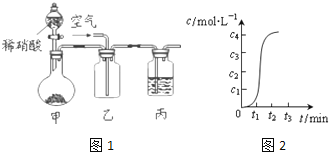
Ⅰ、若将软锰矿和碳反应后的固体产物置于如图1所示的装置甲中,与稀硝酸反应,观察到装置乙中有红棕色气体产生。
(1)写出甲中产生气体反应的化学方程式___。
(2)在制备MnO2的实验中要向反应混合液中不断滴加氨水,则氨水的作用是___。
Ⅱ、有人提出用日光分解KMnO4溶液的方法可制取MnO2,反应方程式为:4KMnO4+2H2O![]() 4MnO2↓+4KOH+3O2↑该反应中c(OH-)随时间的变化曲线如图2所示,分析曲线的变化趋势,你认为形成该变化的原因是___。
4MnO2↓+4KOH+3O2↑该反应中c(OH-)随时间的变化曲线如图2所示,分析曲线的变化趋势,你认为形成该变化的原因是___。
Ⅲ、某兴趣小组通过实验研究MnO2的氧化性进行了一系列的研究。
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是___。
A.把MnO2固体加入到FeSO4溶液中,再加入KSCN溶液,观察溶液是否变红
B.把MnO2固体加入到FeCl3溶液中,再加入KSCN溶液,观察溶液是否变红
C.把MnO2固体加入到Na2SO3溶液中,再加入BaCl2观察是否有白色沉淀生成
D.把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
(2)该小组为研究在不同酸碱性的溶液中MnO2的氧化能力,他们控制KI溶液的浓度和MnO2固体的质量相同,恒定实验温度在298K,设计如下对比试验。
实验 | 酸或碱 | 现象 |
A | 1滴0.2mol/LNaOH溶液 | 不变色 |
B | 1滴水 | 缓慢变浅棕褐色 |
C | 1滴0.1mol/L硫酸溶液 | 迅速变棕褐色 |
该小组从上述对比实验中,可以得出的结论是___。写出在MnO2迅速氧化I的离子方程式___。
【答案】Fe+4HNO3=Fe(NO3)3+NO↑+2H2O 可以中和硝酸,增大反应物的转化率,使原料尽可能多地转化为MnO2 反应生成的MnO2对该反应起催化作用 A 酸性越强,MnO2氧化能力越强 MnO2+2I+4H+= Mn2++I2+2H2O
【解析】
Ⅰ、(1)软锰矿中含有少量Fe2O3,在加热条件下与C反应生成铁,铁与稀硝酸反应生成NO气体,为便于吸收氮氧化物,向乙中通入空气,空气中的氧气将NO氧化成NO2,使气体呈红棕色,丙中应盛NaOH溶液等碱性物质,吸收有毒气体NO2;
(2)制备MnO2的实验中生成HNO3,加入氨水,可以中和硝酸,增大反应物的转化率,使原料尽可能多地转化为MnO2;
Ⅱ、反应中c(OH-)在t1时突然增大,说明反应速率增大,在其它条件不变的情况下,可考虑生成物起催化作用;
Ⅲ、(1) A中,通过溶液变红,可说明MnO2固体将Fe2+氧化为Fe3+;B中,Fe3+没有还原性,MnO2不能表现氧化性;C中,不管是否将SO32-氧化,都产生白色沉淀;D中,MnO2固体加入到稀盐酸中,不发生反应。
(2)从溶液的酸碱性及产生的现象,可得出酸性越强,I-转化为I2的反应速率越快,现象越明显,MnO2氧化能力越强的结论;MnO2在酸性溶液中氧化I,生成Mn2+、I2和H2O。
Ⅰ、(1)软锰矿中含有少量Fe2O3,在加热条件下与C反应生成铁,铁与稀硝酸反应生成NO气体。反应的方程式为Fe+4HNO3=Fe(NO3)3+NO↑+2H2O;答案为:Fe+4HNO3=Fe(NO3)3+NO↑+2H2O;
(2)制备MnO2的实验中生成HNO3,加入氨水,可以中和硝酸,增大反应物的转化率,使原料尽可能多地转化为MnO2;答案为:可以中和硝酸,增大反应物的转化率,使原料尽可能多地转化为MnO2;
Ⅱ、反应中c(OH-)在t1时突然增大,说明反应速率增大,在其它条件不变的情况下,可考虑生成物MnO2起催化作用;答案为:反应生成的MnO2对该反应起催化作用;
Ⅲ、(1) A中,通过溶液变红,可说明MnO2固体将Fe2+氧化为Fe3+,A符合题意;
B中,Fe3+没有还原性,MnO2不能表现氧化性,B不合题意;
C中,不管是否将SO32-氧化,都产生白色沉淀,C不合题意;
D中,MnO2固体加入到稀盐酸中,不发生反应,D不合题意。
故选A;
(2)从溶液的酸碱性及产生的现象,可得出酸性越强,I-转化为I2的反应速率越快,现象越明显,MnO2氧化能力越强的结论;答案为:酸性越强,MnO2氧化能力越强;
MnO2在酸性溶液中氧化I,生成Mn2+、I2和H2O,反应的离子方程式为MnO2+2I+4H+= Mn2++I2+2H2O;答案为:MnO2+2I+4H+= Mn2++I2+2H2O。