题目内容
18.不能用离子方程式CO32-+2H+=H2O+CO2↑表示的反应是( )| A. | K2CO3+2HNO3=2KNO3+CO2↑+H2O | |
| B. | Na2CO3+2HCl=2NaCl+CO2↑+H2O | |
| C. | Ca CO3+2 HCl=CaCl2+CO2↑+H2O | |
| D. | (NH4)2 CO3+H2SO4=(NH4)2 SO4+CO2↑+H2O |
分析 离子方程式CO32-+2H+=H2O+CO2↑表示可溶性碳酸盐与强酸反应生成可溶性盐、二氧化碳气体和水的一类反应,据此对各选项进行判断.
解答 解:A.K2CO3+2HNO3=2KNO3+CO2↑+H2O的离子方程式为CO32-+2H+=H2O+CO2↑,能够用该离子方程式表示,故A错误;
B.Na2CO3+2HCl=2NaCl+CO2↑+H2O的离子方程式为CO32-+2H+=H2O+CO2↑,能够用该离子方程式表示,故B错误;
C.CaCO3+2 HCl=CaCl2+CO2↑+H2O的离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑,不能够用该离子方程式表示,故C正确;
D.(NH4)2CO3+H2SO4=(NH4)2SO4+CO2↑+H2O的离子方程式为CO32-+2H+=H2O+CO2↑,能够用该离子方程式表示,故D错误;
故选C.
点评 本题考查了离子方程式的正误判断,题目难度中等,明确离子方程式表示的意义为巨大的关键,注意掌握离子方程式的书写原则,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
8.氮化硅(Si3N4,其中N元素化合价为-3)是一种具有耐高温、熔融态时不导电等优异性能的新型陶瓷.工业上可用下列方法制取:3SiO2+6C+2N2$\frac{\underline{\;高温\;}}{\;}$ Si3N4+6CO.下列说法不正确的是( )
| A. | 上述反应中,Si元素化合价不变 | B. | 氮化硅晶体中含有Si4+ | ||
| C. | Si3N4属于氮化物 | D. | 上述反应属于氧化还原反应 |
9. 燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.
燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.
(1)对燃煤废气进行脱硝处理时,常利用甲烷催化还原氮氧化物:
①CH4 (g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-570kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1
则CH4 (g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=-865 kJ•mol-1.
(2)将燃煤废气中的CO2转化为甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g)
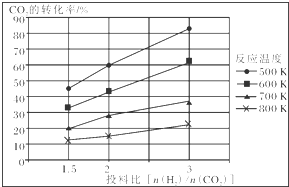
已知在压强为a MPa下,该反应在不同温度、不同投料比时,CO2的转化率见如图:
①此反应为放热(填“放热”、“吸热”);若温度不变,提高投料比[$\frac{n({H}_{2})}{n(C{O}_{2})}$],则K将不变(填“增大”、“减小”或“不变”).
②在a MPa和一定温度下,将6mol H2和2mol CO2在2L密闭容器中混合,当该反应达到平衡时,测得平衡混合气中CH3OCH3的体积分数约为16.7%(即$\frac{1}{6}$),此时CO2的转化率为80%
(3)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
①650℃时该反应的化学平衡常数数值为$\frac{8}{3}$,该反应的逆反应为放(填“吸”或“放”)热反应
②若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),且t<3min,则a、b应满足的关系是b=2a,a>1(用含a、b的数学式表示).
 燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.
燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.(1)对燃煤废气进行脱硝处理时,常利用甲烷催化还原氮氧化物:
①CH4 (g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-570kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1
则CH4 (g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=-865 kJ•mol-1.
(2)将燃煤废气中的CO2转化为甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g)
已知在压强为a MPa下,该反应在不同温度、不同投料比时,CO2的转化率见如图:
①此反应为放热(填“放热”、“吸热”);若温度不变,提高投料比[$\frac{n({H}_{2})}{n(C{O}_{2})}$],则K将不变(填“增大”、“减小”或“不变”).
②在a MPa和一定温度下,将6mol H2和2mol CO2在2L密闭容器中混合,当该反应达到平衡时,测得平衡混合气中CH3OCH3的体积分数约为16.7%(即$\frac{1}{6}$),此时CO2的转化率为80%
(3)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
| 实 验 组 | 温 度 /℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),且t<3min,则a、b应满足的关系是b=2a,a>1(用含a、b的数学式表示).
6.下列溶液中Cl-浓度最大的是( )
| A. | 200mL 2 mol•L-1 MgCl2溶液 | B. | 1000mL 2.5 mol•L-1 NaCl溶液 | ||
| C. | 300mL 5 mol•L-1 KCl溶液 | D. | 250mL 1 mol•L-1 AlCl3溶液 |
10.维生素通常根据他们的溶解度来进行分类,它们或者溶解在水中或者溶解在脂肪中.下列维生素中属于水溶性维生素的是( )
| A. | 维生素A | B. | 维生素C族 | C. | 维生素D | D. | 维生素E |
7.含有大量Ba2+、OH-、NO3-的溶液中还可能大量存在的离子是( )
| A. | Na+ | B. | H+ | C. | SO42- | D. | Mg2+ |
8.下列实验操作正确的是( )
| A. | 分液时,分液漏斗内上层液体从上口倒出,下层液体从下口倒出 | |
| B. | 过滤时,为加快过滤速度,应用玻璃棒不断搅拌 | |
| C. | 对于互溶的且沸点相差较大的两种液体,可使用蒸馏的方法分离 | |
| D. | 将硫酸铜晶体置于蒸发皿中加热,令其失去结晶水 |
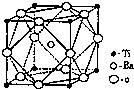 钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题: